(9分)有两个实验小组的同学探究一氧化碳、二氧化硫与过氧化钠的反应。请回答下列问题:
(1)第一小组同学设计如图装置进行实验。通入SO2气体,将带余烬的木条插入试管C中,木条复燃。
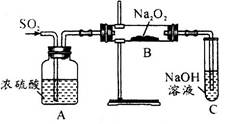
甲同学认为Na2O2与SO2反应生成了Na2SO3和O2,则反应的化学方程式为___________________________。
乙同学认为Na2O:与SO2反应除了生成Na2SO3和O2外,还有Na2SO4生成。为检验是否有Na2SO4生成,该同学设计了如下方案:
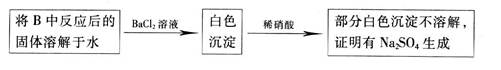
你认为乙同学的方案是否合理____________(答“是”或“否”);请简要说明两点理由:
①__________________________________________________________________________
②__________________________________________________________________________.
(2)第二小组同学利用下图中的有关装置(固定装置及胶管略去)验证CO气体能否与Na2O2反应。已知:H2C2O4  CO2↑+CO↑+H2O
CO2↑+CO↑+H2O
(乙二酸)
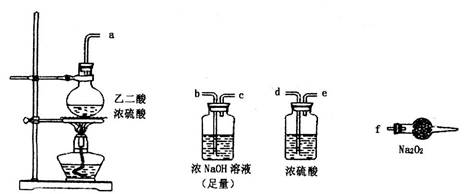
若CO能够与Na2O2发生反应,则预测反应产物为______________________;验证该产物可选择的试剂是___________________________________________________。
上述实验中选择的最简单的装置接口连接顺序为_________________________.
(1)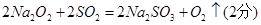 ;否(1分)
;否(1分)
①稀HNO3可以把BaSO3氧化为BaSO4(1分)
②若反应后的固体有Na2O2残留,溶于水后可把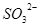 氧化为
氧化为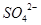 (1分)
(1分)
(2)Na2CO3(1分);稀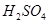 (或稀HC1)和澄清石灰水(1分);a b c f(2分)
(或稀HC1)和澄清石灰水(1分);a b c f(2分)
(1)仿照CO2与过氧化钠的反应方程式可写出或直接配平: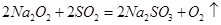
(2)本质是检验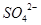 的存在,该方案明显不合理:
的存在,该方案明显不合理:
①原溶液中即使没有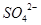 ,但
,但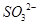 与加入的氯化钡溶液形成的BaSO3可被稀HNO3氧化为BaSO4
与加入的氯化钡溶液形成的BaSO3可被稀HNO3氧化为BaSO4
②若反应后的固体有Na2O2残留,溶于水后可把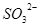 氧化为
氧化为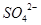 ,最终也可以得到同样的现象
,最终也可以得到同样的现象
正确的检验过程是:先加入过量盐酸,再加入氯化钡溶液,如果有白色沉淀生成,则可证明有Na2SO4存在
(2)CO被Na2O2氧化:Na2O2+CO=Na2CO3
Na2CO3属于碳酸盐,可用酸与其反应产生CO2,再通入澄清石灰水中,看是否有浑浊出现;
由于H2C2O4  CO2↑+CO↑+H2O,产生的CO中含有CO2,故应先用碱液吸收CO2,则装置接口的连接顺序为:a b c f
CO2↑+CO↑+H2O,产生的CO中含有CO2,故应先用碱液吸收CO2,则装置接口的连接顺序为:a b c f
