问题
实验题
(12分)
已知HI是一种无色,有刺激性气味,极易溶于水的气体,HI的水溶液称之为氢碘酸,是一种强酸。
(1)请写出I元素在周期表的位置:第五周期 族
(2)将HI气体通入一定量的浓硫酸中,产生的混合气体除含HI、少量的I2蒸气和水蒸气外,还可能有 气体。
(3) 小明拟对HI通入浓硫酸后的混合气体成分进行验证和探究。他设计了如下实验装置图
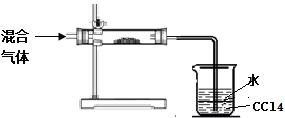
初步探究设计:
①其中直形玻璃管中所装的药品是 (写名称)
②足量四氯化碳的两个作用是:  。
。
进一步探究:
查阅资料:氧化性强弱KMnO4>HNO3>I2>SO42-,且较稀的硝酸不能氧化I2。
③小明拟对溶在水层的其它混合气体成分做进一步探究。请你从以下限选试剂中选择合适的试剂帮小明完成实验报告。
限选的试剂:石蕊试剂、品红溶液、酸性KMnO4溶液、0.1mol/L HNO3、淀粉溶液、BaCl2溶液
| 实验方案 | 可能的现象和相应的结论 |
| 取少量烧杯中的上层溶液分装入A、B两支试管中 | |
答案
(12分)
(1) VIIA(1分)  (2) SO2(2分)
(2) SO2(2分)
(3) ①无水硫酸铜(2分)
②检验、吸收碘蒸气;防倒吸(2分,每个1 分)
分)
③(答案合理便给分)
| 实验方案 | 可能的现象和相应的结论 |
| 往A试管中加入少量品红溶液 (1分) | 若品红溶液褪色,则原混合气体中有SO2 若溶液不褪色,则原混合气体中没有SO2(1分) |
| 往B试管中滴加足量硝酸溶液后(1分),再滴入少量淀粉溶液(1分) | 若淀粉溶液变蓝,则原混合气体中有HI 若溶液不变蓝,则原混合气体中没有HI(1分) |
