(14分)下图中,A、B、C、D、E是单质,G、H、I、F是B、C、D、E分别和A形成的二元化合物。已知:①反应C+G B+H能放出大量的热,该反应曾应用于铁轨的焊接;②I是一种常见的温室气体,它和E可以发生反应:2E+I
B+H能放出大量的热,该反应曾应用于铁轨的焊接;②I是一种常见的温室气体,它和E可以发生反应:2E+I 2F+D,F中E元素的质量分数为60%。
2F+D,F中E元素的质量分数为60%。
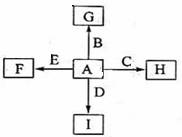
回答问题:
⑴①中反应的化学方程式为 ;
⑵化合物I的电子式为 ,它的空间结构是 ;
⑶将G溶于盐酸,得到的溶液加入一定量的铜粉,写出离子方程式:
⑷C与过量NaOH溶液反应的离子方程式为 ,反应后溶于与过量化合物I反应的离子方程式为 ;
⑸E在I中燃烧观察到的现象是 。
(1)8Al+3Fe3O4 9Fe+4Al2O3
9Fe+4Al2O3
(2)  直线形 (3) 2Fe3++Cu=2Fe2++Cu2+
直线形 (3) 2Fe3++Cu=2Fe2++Cu2+
(4)2Al+2OH-+2H2O=2AlO-2+3H2↑
AlO2-+CO2+2H2O=Al(OH)3↓+HCO3- (注:不要求写OH-+CO2=HCO-3)
(5)镁条剧烈燃烧,生成白色粉末,反应器内壁附有黑色的碳
根据①可知,这是铝热反应,所以C是铝,则H是氧化铝,A是氧气,G是四氧化三铁,B就是铁。常见的温室气体是CO2,所以I是CO2,则D是碳。能在CO2中燃烧,能把CO2中的碳置换出来的是镁,即E是镁,F是氧化镁,氧化镁中镁元素的质量分数是60%。
