(15 分) S2Cl2是工业上常用的硫化剂,实验室制备S2Cl2的反应原理有两种:
① CS2+3Cl2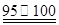 ℃CCl4+S2Cl2;② 2S+Cl2
℃CCl4+S2Cl2;② 2S+Cl2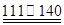 ℃S2Cl2。
℃S2Cl2。
已知:S2Cl2易与水反应,S2Cl2+Cl2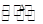 2SCl2。
2SCl2。
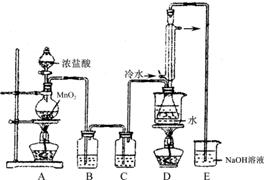
下列是几种物质的熔沸点和反应装置图
| 物质 | 沸点/℃ | 熔点/℃ |
| S | 445 | 113 |
| CS2 | 47 | -109 |
| CCl4 | 77 | -23 |
| S2Cl2 | 137 | -77 |
(2)若装置C更换成干燥管,则装置C中可选用的固体试剂是 。
(3)D装置中冷凝管的作用是 ;反应结束后,将D装置锥形瓶内的混合物中分离出产物的方法是 。
(4)S2Cl2与足量水反应有黄色沉淀生成,产生的无色气体能使品红溶液褪色,则该反应的化学方程式为 。
(5)为了提高制得的产品S2Cl2的纯度,关键的操作是控制好温度和 。
(6)上图尾部装置不够完善,存在的问题是 。
(15 分)
(1)①。(2分)
(2)无水氯化钙或固体五氧化二磷。(2分)
(3)冷凝回流、导气。(各1分,共计2分) 蒸馏 (2分)
(4)2S2Cl2+2H2O=3S↓+SO2↑+4HCl(2分)
(5)控制浓盐酸的滴速不要过快(2分)
(6)在D和E之间增加干燥装置、尾气吸收要防止倒吸(3分,少一个扣2分)
题目分析:(1)图中D装置是液体与液体的反应,故反应原理是①。
(2)注意C装置中的固体不能与2Cl2反应,故装置C中可选用的固体试剂是无水氯化钙或固体五氧化二磷。
(3)D装置中冷凝管是冷凝Cl2的温度,故作用是冷凝回流、导气。CS2与S2Cl2沸点的相差很大,故分离的方法是蒸馏。
(4)S2Cl2与足量水反应有黄色沉淀生成,产生的无色气体能使品红溶液褪色,说明生成了固体S和SO2气体,故方程式为2S2Cl2+2H2O=3S↓+SO2↑+4HCl。
(5)为了提高制得的产品S2Cl2的纯度,需要控制好温度和使反应物混合均匀充分反应,故填空为控制浓盐酸的滴速不要过快。
(6)E装置容易倒吸,故存在的问题是在D和E之间增加干燥装置、尾气吸收要防止倒吸。
点评:本题是有关实验方案的设计和评价的考查,要求学生熟悉所实验的内容及原理,能够考查同学们进行分析问题、解决问题的能力。
