(12分)某学生实验兴趣小组拟用图1装置来完成“NaHCO3和NaCl混合物中NaHCO3含量的测定”的实验。
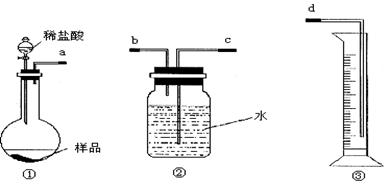
图1
(1)各仪器接口连接顺序是_________________(用接口字母填写)。
(2)该装置连接好而未装药品前,检验气密性的操作是_________________________。
(3)甲同学认为上述方法误差较大,提出如下改进措施,你认为可行的有______。(填序号)
A.在滴入盐酸之前,应排净装置内的CO2气体
B.在装置①中稀盐酸换成稀硫酸,装置②中水换成饱和NaHCO3溶液
C.在装置②中水换成饱和Na2CO3溶液
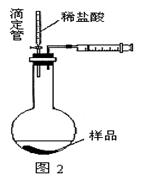
D.滴加盐酸不宜过快(4)乙同学认为在装置②③之间的导管内会积存水,使测定结果不准,从而改用图2装置。假定滴定管起始读数为V1mL,终了读数为V2mL,而注射器测定排出的气体为V3mL(标准状况下),混合物样品质量为m g,则原混合物中NaHCO3的质量分数的表达式为_______。
(用含V1、V2、V3、m的式子表示)。
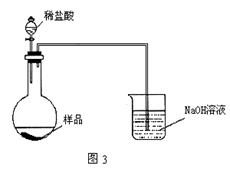
(5)丙同学改用图3装置,通过测定烧杯的质量。你认为乙、丙两同学的方案中,谁的方案更合理__________,理由是:_____________。
(1)a、b、c、d(2分)
(2)答案1:在②中加水浸没长导管,关闭分液漏斗活塞,用手握住圆底烧瓶(或酒精灯微热),若②中长导管内液面上升,则说明气密性好;答案2:在③中加水浸没导管,关闭分液漏斗活塞,用酒精灯微热,若③中导管口产生均匀的气泡,停止加热后,导管末端形成一段水柱且保持一段时间不下降,则说明气密性好。(2分)
(3)BD(2分)
(4)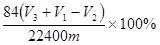 (2分)
(2分)
(5)乙同学(1分)丙同学的方案中,生成的CO2没有全被NaOH溶液吸收。(2分)
(1)根据实验装置图可知,是利用通过排水法测量水的体积,进而得出气体的体积,实验正确的顺序是a、b、c、d。
(2)根据装置的特点可知,检验方法是在②中加水浸没长导管,关闭分液漏斗活塞,用手握住圆底烧瓶(或酒精灯微热),若②中长导管内液面上升,则说明气密性好;或在③中加水浸没导管,关闭分液漏斗活塞,用酒精灯微热,若③中导管口产生均匀的气泡,停止加热后,导管末端形成一段水柱且保持一段时间不下降,则说明气密性好。
(3)由于反应后装置中会残留部分CO2气体,所以反应前没有必要排净装置内的CO2气体。由于CO2能和碳酸钠溶液反应,所以C也不正确,因此正确的答案是BD。
(4)根据体积的变化可知,生成的CO2是V3-(V2-V1)=V3+V1-V2,其物质的量是(V3+V1-V2)/22400mol,所以碳酸氢钠的质量是84(V3+V1-V2)/22400g,因此质量分数是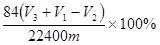 。
。
(3)根装置③的结构可知,反应中产生的CO2不可能完全被氢氧化钠溶液吸收,测定结果偏低,所以不如装置②好。
