某校研究性学习小组选择使用下列仪器和药品,验证由铜和适量浓硝酸反应产生的气体中含有NO(实验中使用的N2和O2的用量可自由控制)。
已知:①NO + NO2 + 2OH-=2NO2-+H2O ②气体液化温度:NO2:21℃、NO:-152℃
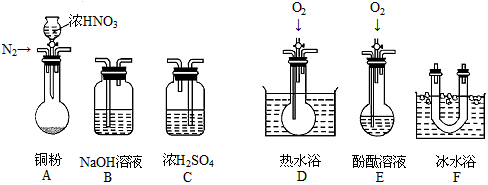
(1)现有甲、乙、丙三位同学分别设计了以下三个实验方案(用仪器的连接顺序表示)。
甲:A→C→F→D→B 乙:A→B→C→E 丙:A→F→D→B
甲、乙、丙三位同学提出的实验方案是否能验证Cu与适量浓HNO3反应产生的气体中含有NO(填“能”或“不能”)甲:________;乙:________;丙:_________ 用化学方程式表示不能验证的主要原因(若三个实验方案都能验证,则此小题不用回答):
甲方案:_______________________________
乙方案:_______________________________
丙方案:_______________________________
(2)实验开始时首先通入足量的N2,其目的是:_______________________________。
(3)确认气体中含NO的现象是:______________________________________________。
(4)如果O2过量,则装置B中发生反应的离子方程式是:__________________________。
(1)甲:能;乙:不能;丙:不能
乙方案:混合气体在通过B时,因发生反应:NO+NO2+2NaOH==2NaNO2+H2O使NO消耗,后续实验无法验证是否有NO
丙方案:混合气体通过F时,NO2与H2O蒸气发生反应:3NO2+H2O==2HNO3+NO 使部分NO2转化为NO,产生干扰,从而不能确认Cu和浓HNO3反应是否有NO生成
(2)排尽整个装置中的空气,防止产生的NO被氧化生成NO2
(3)D装置中通入O2后有红棕色气体产生
(4)4NO2+O2+4OH-==4NO3-+2H2O
