科研人员将软锰矿(MnO2含量≥65%,SiO2含量约20%,A12O3含量约4%,其余为水分)和闪锌矿(ZnS含量≥80%,FeS、CuS、SiO2含量约7%,其余为水分)同槽酸浸开发出综合利用这两种资源的新工艺,如图所示为工艺流程的一部分.
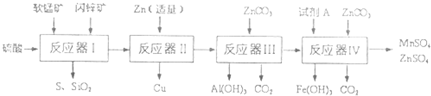
已知:ZnCO3不溶于水,但溶于酸.部分阳离子以氢氧化物形式深沉时溶液的pH见下表:
| 物质 | Fe(OH)3 | A1(OH)3 | Zn(OH)2 | Fe(OH)2 | Mn(OH)2 |
| 开始沉淀pH | 2.7 | 3.3 | 5.4 | 7.6 | 8.3 |
| 完全沉淀pH | 4.4 | 5.2 | 8.0 | 9.6 | 9.8 |
(1)反应器I过滤所得滤液中含有MnSO4、ZnSO4、CuSO4、Fe2(SO4)3、A12(CO4)3等.试完成反应器I中生成CuSO4的化学方程式(不须配平):CuS+______+H2SO4→______+______+CuSO4+H2O
(2)反应器II中发生反应的离子方程式为______.
(3)从沉淀溶解平衡的角度分析反应器III中生成A1(OH)3沉淀的原因______.检验ZnCO3是否过量的操作方法是______.
(4)反应器中IV中,试剂A可以是下列物质中______(填代号).a.氨水 b.氢氧化钠 c.MnO2 d.稀硫酸
(5)欲从反应器IV的滤液中完全沉淀出Zn(OH)2,而不析出Mn(OH)2,则滤液的pH范围为______,要将分离出沉淀后的滤液进行浓缩,需将温度控制在90℃~100℃,可采用的加热方法是______.
(1)反应I为酸浸过程,Mn、Al、Zn、Fe、Cu元素在该过程均转化为金属阳离子进入溶液,而难溶于酸的S、SiO2则通过过滤而分离出来,
故答案为:MnO2;S↓;MnSO4;
(2)加入Zn后,Zn把Cu置换出来,而且Zn还原Fe3+,发生氧化还原反应.故答案为:Zn+2Fe3+=2Fe2++Zn2+、Zn+Cu2+=Cu+Zn2+;
(3)加入ZnCO3后,ZnCO3与溶液中的H+反应,导致溶液中c(H+)减小,c(OH-)增大,c(Al3+)•c(OH-)>Ksp[Al(OH)3],从而生成Al(OH)3沉淀;取少许沉淀于试管中,滴加适量的稀硫酸,若有气泡产生,则说明ZnCO3过量;若无气泡产生,则说明ZnCO3不过量.故答案为:ZnCO3与溶液中的H+反应,导致溶液中c(H+)减小,c(OH-)增大,从而生成Al(OH)3沉淀;取少许沉淀于试管中,滴加适量的稀硫酸,若有气泡产生,则说明ZnCO3过量;若无气泡产生,则说明ZnCO3不过量.
(4)在所得虑液中加入MnO2将Fe2+氧化为Fe3+,再加入ZnCO3调节溶液pH 在5.2-5.4之间使Fe3+、Al3+完全转化为Fe(OH)3、Al(OH)3而分离(超过5.4Zn(OH)2会析出).故选c;
(5)从反应器IV的滤液中完全沉淀出Zn(OH)2,而不析出Mn(OH)2,则滤液的pH范围为8.0≤pH<8.3(超过8.3Mn(OH)2会析出);将温度控制在90℃~100℃,最好采用水浴加热.故答案为:8.0≤pH<8.3;水浴加热.
