问题
实验题
某学生为了探究锌与盐酸反应过程中的速率变化,他在100mL稀盐酸中加入足量的锌粉,用排水集气法收集反应放出的氢气,实验记录如下(累计值,体积已换算成标准状态))
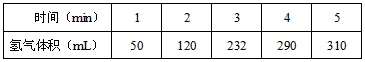
(1)哪一时间段___________(指0~1、1~2、2~3、3~4、4~5 min)反应速率最大,原因是_____________。
(2)哪一段时段的反应速率最小__________________,原因是_________________________。
(3)求2~3分钟时间段以盐酸的浓度变化来表示的该反应速率(设溶液体积不变)______________。
(4)如果反应太激烈,为了减缓反应速率而又不减少产生氢气的量,他在盐酸中分别加入等体积的下列溶液:A.蒸馏水 B.NaCl溶液 C.Na2CO3溶液 D.CuSO4溶液
你认为可行的是(填编号)________________。
答案
(1)2~3min;因为该反应是放热反应,2~3min时温度高
(2)4~5min;因为4~5min是H+浓度小
(3)0.1 mol/(L·min)
(4)AB
