某课外兴趣小组探究铝与盐酸反应的反应速率与哪些因素有关。
请填写下列空白:
(1)实验化学反应原理:______________________ 。
(2)实验用品:试管(普通试管和具支试管各一支)、镊子、乳胶管、玻璃导管、水槽、;稀盐酸(4mol/L)、铝条(片)、水、胶头滴管、温度计。
(3)实验装置 (图中铁架台等夹持仪器略去)
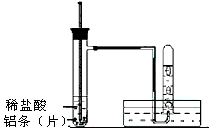
(4)实验方法
①按如上图所示连接好实验仪器,检查装置的气密性,具体操作方法是:__________________ 。
②取3块铝条(足量)加入到试管中。
③在盛有铝条的试管中,加入2mL稀盐酸。
④测量试管中溶液的温度。
⑤收集反应产生的氢气。
(5)数据处理及问题讨论
①实验结束后,课外兴趣小组成员将产生氢气的体积与时间作了如下的图。
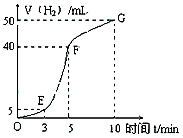
②试判断OE、EF、FG段所收集气体的多少。
OE:__________ ;EF:__________ ;FG:______________ 。写出这三段时间内产生氢气的速率大小比较(用OE、EF、FG 表示),并解释原因速率大小比较:_______________ 。原因:________
③如果反应太激烈,为了减缓反应速率而又不减少产生氢气的量,他在盐酸中分别加入下列溶液:
A.蒸馏水
B.NaCl溶液
C.Na2CO3溶液
D.CuSO4溶液
E.NaNO3溶液
你认为可行的是________________________(填编号) 。
(1)2Al+6HCl=2AlCl3+3H2↑
(4)①将导气管口放入水槽的水中,用手握住具支试管一会儿,如果导气管中有气泡冒出,移开手后,导气管中有一段水柱上升,且水柱在较长时间内不回落,即证明该装置气密性良好。
(5)5mL;35mL;10mL;EF>FG>OE;该反应是放热反应,随着温度的升高,反应速率增大,一段时间后,随着反应物的浓度的减小,反应速率减小;A、B

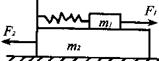
 的左端,右端与小木块
的左端,右端与小木块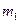 连接,且
连接,且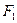 和
和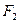 ,从两物体开始运动以后的整个过程中,对
,从两物体开始运动以后的整个过程中,对