已知难溶电解质在水溶液中存在溶解平衡:MmAn(s)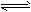 mMn+(aq)+nAm-(aq),Ksp=[Mn+]·[Am-]n,称为溶度积。某学习小组欲探究CaSO4沉淀转化为CaCO3沉淀的可能性,查得如下资料:(25℃)
mMn+(aq)+nAm-(aq),Ksp=[Mn+]·[Am-]n,称为溶度积。某学习小组欲探究CaSO4沉淀转化为CaCO3沉淀的可能性,查得如下资料:(25℃)

实验步骤如下:
①往100 mL 0.1 mol·L-1的CaCl2溶液中加入100 mL 0.1 mol·L-1的Na2SO4溶液,立即有白色沉淀生成。
②向上述悬浊液中加入固体Na2CO3 3g,搅拌,静置,沉淀后弃去上层清液。
③再加入蒸馏水搅拌,静置,沉淀后再弃去上层清液。
④_________________________。
(1)由题中信息Ksp越大,表示电解质的溶解度越______(填“大”或“小”)。
(2)写出第②步发生反应的化学方程式:__________________________。
(3)设计第③步的目的是____________________。
(4)请补充第④步操作及发生的现象:__________________________________。
(1)大
(2)Na2CO3+CaSO4==Na2SO4+CaCO3
(3)洗去沉淀中附着的SO42-
(4)向沉淀中加入足量的盐酸,沉淀完全溶解