为了探究草酸(H2C2O4)的化学性质,设计如下3个实验:
实验1:取一定量草酸溶液装入试管,加入一定体积的酸性高锰酸钾溶液,振荡试管,发现溶液开始缓慢褪色,后来迅速变成无色。(反应热效应不明显,可忽略不计)
(1)该实验说明草酸具有________(填“氧化”或“还原”)性,该反应的反应速率先慢后快的主要原因可能是__________________。
实验2:取少量草酸晶体装入试管,加水溶解,向试管里滴加足量的澄清石灰水,有白色沉淀生成。
(2)该实验说明草酸具有______性。写出反应的化学方程式:__________________。
实验3:草酸在常温下呈无色晶体状,其晶体的熔化温度低于草酸的分解温度,且易升华。为了探究草酸的不稳定性,某同学设计如下实验装置
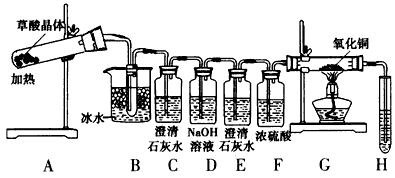
(3)B装置的作用是__________________。C装置变浑浊,E处无现象,G玻璃管里黑色变红色,写出A中反应的化学方程式:__________________。
(4)为了检验G中反应的氧化产物,H试管所装试剂是___________,从环境保护角度来看,该方案的不足之处是________________________。
(1)还原;锰离子起催化作用或锰离子浓度增加,加快了反应速率
(2)酸;Ca(OH)2+H2C2O4=CaC2O4↓+2H2O
(3)冷凝草酸蒸气,避免对二氧化碳的检验产生干扰;H2C2O4 CO↑+CO2↑+H2O
CO↑+CO2↑+H2O
(4)澄清石灰水(或偏铝酸钠溶液或硅酸钠溶液等);没有尾气处理装置
