研究性学习小组进行SO2的制备及性质探究实验。
(1)根据反应Na2SO3(固)+H2SO4(浓)==Na2SO4+SO2↑+H2O,制备SO2气体。
①用简图(下图)在方框中画出制备并收集SO2的实验装置(含试剂)示意图。
②实验过程中,使用分液漏斗滴加浓硫酸的操作是__________________。
(2)将SO2气体分别通入下列溶液中:
①品红溶液,现象是________________________;
②溴水溶液,现象是________________________;
③硫化钠溶液,现象是______________________。
(3)有一小组在实验中发现,SO2气体产生缓慢,以致后续实验现象很不明显,但又不存在气密性问题。请你推测可能的原因并说明相应的验证方法(可以不填满)。
①原因________________,验证方法____________________________。
②原因________________,验证方法____________________________。
③原因________________,验证方法____________________________。
(1)①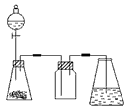
②打开分液漏斗上口的活塞,旋开分液漏斗的旋塞,缓慢滴加
(2)①溶液褪色;②溶液褪色;③有浅黄色沉淀生成(或溶液变浑浊)
(3)①Na2SO3变质;取待测试样于试管中,加适量蒸馏水配成溶液,先滴入足量稀盐酸,再滴入BaCl2溶液,有白色沉淀生成,则证明该Na2SO3固体变质
②所用硫酸不是浓硫酸 用干燥洁净的玻璃棒蘸取待测试样,涂在白纸上,白纸不变黑,则证明该溶液不是浓硫酸
