化学反应在工农业生产中有着重要的应用。按要求回答下列问题:
(1)利用化学反应可以制备许多物质。
①实验室用铜制备NO的离子方程式为___________________。
②可用Al和Fe2O3制Fe,该反应的化学方程式为___________________。
③海水提溴过程中,向浓缩的海水中通入氯气,再用热空气吹出生成的溴,然后用碳酸钠溶液吸收溴,溴歧化为Br-和BrO3-。这两步反应的离子方程式分别为__________、___________。
(2)化学反应能为人类生产生活提供能源。
①由反应CH4 +2O2 CO2 +2H2O,可以设计出以NaOH溶液为电解质溶液的燃料电池,该电池工作时负极的电极反应式为:______________。
CO2 +2H2O,可以设计出以NaOH溶液为电解质溶液的燃料电池,该电池工作时负极的电极反应式为:______________。
②2011年山东高考化学中曾提到钠硫高能电池,右图是该电池的结构示意图,该电池的工作温度为320℃左右,电池反应为2Na+xS=Na2Sx。该电池负极为________(填化学式),正极的电极反应式为 。用该电池作电源进行粗铜精炼时,当得到64g精铜时,理论上该电池负极消耗的质量为_____g。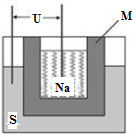
(1)①3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O
②2Al+Fe2O3 2Fe+Al2O3;(缺少条件减1分)
2Fe+Al2O3;(缺少条件减1分)
③2Br-+Cl2=2Cl-+Br2,3Br2+3CO32-=5Br-+BrO3-+3CO2↑
(2)①CH4+10OH--8e-=CO32-+7H2O;②Na,xS+2e-=Sx2-,46
题目分析:(1)①硝酸具有强氧化性,能和金属铜发生氧化还原反应,因此可用于稀硝酸与铜反应制备NO,反应的离子方程式为3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O。
②铝是活泼的金属,可以通过铝热反应冶炼金属,所以可用Al和Fe2O3制Fe,该反应的化学方程式为2Al+Fe2O3 2Fe+Al2O3。
2Fe+Al2O3。
③氯气氧化性强于单质溴的,所以氯气能把溴离子氧化生成单质溴,反应的离子方程式为2Br-+Cl2=2Cl-+Br2。单质溴溶于水显酸性,能和碳酸钠溶液发生歧化反应生成NaBr、NaBrO3和水,反应的离子方程式为3Br2+3CO32-=5Br-+BrO3-+3CO2↑。
(2)①原电池中负极失去电子,发生氧化反应。正极得到电子发生还原反应,则根据反应CH4 +2O2 CO2 +2H2O可知,还原剂是甲烷,氧气是氧化剂,所以如果设计成原电池,则氧气在正极通入,甲烷在负极通入。由于电解质溶液是氢氧化钠溶液,所以负极电极反应式为CH4+10OH--8e-=CO32-+7H2O。
CO2 +2H2O可知,还原剂是甲烷,氧气是氧化剂,所以如果设计成原电池,则氧气在正极通入,甲烷在负极通入。由于电解质溶液是氢氧化钠溶液,所以负极电极反应式为CH4+10OH--8e-=CO32-+7H2O。
②原电池中负极失去电子,发生氧化反应。正极得到电子发生还原反应,则根据电池反应为2Na+xS=Na2Sx可知,钠是还原剂,所以该电池负极为Na。正极是S得到电子,则正极电极反应式为xS+2e-=Sx2-。64g铜的物质的量=64g÷64g/mol=1mol,根据电极反应式Cu2++2e-=Cu可知,转移2mol电子,所以根据电子守恒可知,负极消耗金属钠的物质的量是2mol,质量=2mol×23g/mol=46g。
