某研究性学习小组探究甲醛与新制的氧化铜反应的产物。
【实验操作】取一支试管,加入2mL20﹪的氢氧化钠溶液,滴入4滴饱和硫酸铜溶液,再加入2mL 37%~40%的甲醛溶液,振荡后放入60℃左右的热水浴中加热。
【实验现象】溶液变浑浊,有暗红色固体生成,且有气泡产生。
Ⅰ探究暗红色固体的成分.
【提出假设】
假设l:暗红色固体为Cu
假设2;暗红色固体为Cu2O
假设3:暗红色固体为____________________________。
【查阅资料】Cu2O能溶解于氨水,形成无色溶液,并很快被空气中氧气氧化为蓝色溶液;
Cu不能溶解于氨水。
【实验验证】

Ⅱ探究气体产物X的成分。为进一步探究实验中气体产物X的成分,甲同学按相同比例取较多量试剂从新进行实验,并将产生的气体通入下列装置中
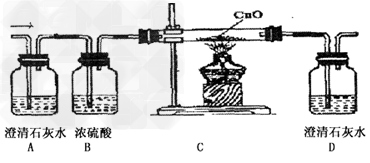
实验中,A装置中没有明显现象,C装置中黑色粉末变红,D装置中溶滚变浑浊,可以推断气体产物X含有_________________(填化学式)。
【思考与交流】
(1)A装置的作用有_________________ 和_________________。
(2)乙同学提出,上述装置有明显的不足,请你指出该不足之处________________
(3)丙同学提出:在该实验条件下,气体产物X中不可能含有CO2。你认为他的理由是_________________________________。
Ⅰ假设3:Cu 和Cu2O
实验验证:固体部分溶解,溶液很快变蓝色
ⅡCO ;
思考与交流:(1)检验气体中是否含有CO2;除去可能挥发出的HCHO蒸气
(2)没有尾气处理装置;(3)反应液呈碱性,不可能有CO2气体溢出
