用下图所示装置进行实验(夹持装置已略去)。请回答下列问题:
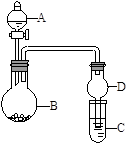
(1)若A中为浓硝酸,B中为铜单质,C中为氢氧化钠溶液。现将浓硝酸滴入B中,则B中发生反应的化学方程式为 。
(2)若A中为浓氨水,B中为生石灰,C中为明矾溶液。
①将浓氨水逐滴滴入B中,可产生大量氨气,原因可能是 _ (填序号)。
a.生石灰和浓氨水反应产生氨气,氨气易溶于水
b.生石灰和水反应,消耗水,使氨气的溶解量减少
c.反应放出大量热,使氨气在水中溶解度明显降低
② C中通入过量氨气时,反应的离子方程式为 。
(3)若A中为水,B中为过氧化钠,C中为酸性淀粉碘化钾溶液,将水滴入B中后,B中的实验现象为 ;若C中溶液变为蓝色,则C中发生反应的离子方程式为_ 。
(1)Cu + 4HNO3(浓) = Cu(NO3)2+ 2NO2↑+ 2H2O (2)①b c(每个1分,共2分) ②3NH3 + 3H2O + Al3+ = Al(OH)3↓ + 3NH4+(或3NH3·H2O + Al3+ = Al(OH)3↓ + 3NH4+) (3)有无色气泡产生 O2 + 4I- + 4H+ = 2I2 + 2H2O
题目分析:(1)浓硝酸和铜发生氧化还原反应有二氧化氮气体生成,则B中发生反应的化学方程式为Cu + 4HNO3(浓) = Cu(NO3)2+ 2NO2↑+ 2H2O。(2)①将浓氨水逐滴滴入B中,可产生大量氨气,主要原因应该是 生石灰和水反应,消耗水,使氨气的溶解量减少,另外反应放出大量热,使氨气在水中溶解度明显降低,故选bc。② 氢氧化铝不能在弱碱中溶解,通入过量氨气时,反应的离子方程式为3NH3 + 3H2O + Al3+ = Al(OH)3↓ + 3NH4+(或3NH3·H2O + Al3+ = Al(OH)3↓ + 3NH4+)。(3)水和过氧化钠反应会生成氧气,另外氧气能氧化碘离子为碘分子,碘与淀粉变为蓝色,因此B中的实验现象为有无色气泡产生;若C中溶液变为蓝色,则C中发生反应的离子方程式为O2 + 4I- + 4H+ = 2I2 + 2H2O 。
