某同学为研究硫酸的性质,设计了以下实验。检查好 装置的气密性后,在甲的试管中加入足量的Fe和少量的C,然后,加入少量浓硫酸。
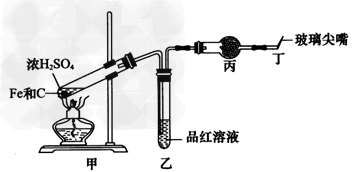
(1)在未点燃酒精灯时,乙中没有明显现象,这是因为___________,为处理生成的有毒气体,干燥管丙中应填充足量的____________。
(2)反应过程中甲中可能发生的反应为:__________(写化学反应方程式)。
(3)接入该仪器后,点燃酒精灯,反应开始一段时间后,在丁处 检验到某种无色无味气体,它是__________;由于甲中加入了单 质碳,使丁处产生气体的速率比不加入时快,这是因为____________。
(4)反应结束后,甲装置的试管中的溶液里存在的溶质是____________。
(1)未加热时,铁在浓H2SO4中会发生钝化且C与浓H2SO4不反应,故没有SO2生成 ;碱石灰
(2)2Fe+6H2SO4(浓)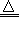 Fe2(SO4)3+3SO2↑+6H2O
Fe2(SO4)3+3SO2↑+6H2O
C+2H2SO4(浓) 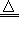 2SO2↑+CO2↑+2H2O
2SO2↑+CO2↑+2H2O
Fe2(SO4)3+Fe=3FeSO4
Fe+H2SO4(稀)=FeSO4+H2↑
(3) H2 ;Fe、C与稀H2SO4构成了原电池
(4)FeSO4
