问题
填空题
研究NO2、SO2、CO等大气污染物气体的处理具有重要意义。
(1)已知:2SO2(g)+O2(g) 2SO3(g);△H= -Q1KJ·mol-1
2SO3(g);△H= -Q1KJ·mol-1
2NO(g)+O2(g)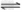 2NO2(g);△H= -Q2KJ·mol-1
2NO2(g);△H= -Q2KJ·mol-1
则反应NO2(g)+SO2(g)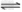 SO3(g)+NO(g);△H= ________KJ·mol-1
SO3(g)+NO(g);△H= ________KJ·mol-1
(2)一定条件下,将NO2与SO2以体积比1︰2置于密闭容器中发生上述反应,当平衡时NO2与NO体积比为1︰3,则平衡常数K=________ 。
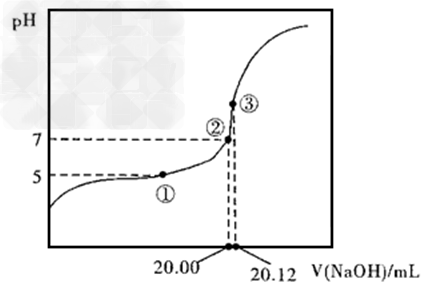
(3)CO可用于合成甲醇,反应方程式为:CO(g)+2H2(g)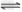 CH3OH(g)。CO在不同温度下的平衡转化率与压强的关系如下图所示,则该反应△H= _____0 (填“>” 或“<” )。实际生产条件下控制在250℃、1.3×104kPa左右,选择此条件下的理由是__________ 。
CH3OH(g)。CO在不同温度下的平衡转化率与压强的关系如下图所示,则该反应△H= _____0 (填“>” 或“<” )。实际生产条件下控制在250℃、1.3×104kPa左右,选择此条件下的理由是__________ 。
答案
(1)-(Q1-Q2)/2或(Q2-Q1)/2
(2)1.8
(3)<;该反应是放热反应,降低温度,有利于甲醇合成,在250℃、1.3×104kPa下,CO的转化率已经很高,增加压强CO的转化率提高不大,而生产成本却会显著增加(或经济效益不好)
