硫酸亚锡(SnSO4)、四氯化锡(SnCl4)常用于印染和电镀工业。
(1)某研究小组设计SnSO4制备路线如下:
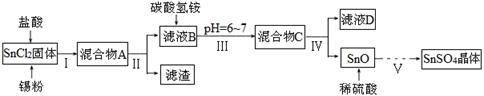
已知:酸性条件下,锡在水溶液中有Sn2+、Sn4+两种主要存在形式,Sn2+易被氧化;SnCl2极易水解。
①SnCl2酸溶后加入Sn粉的作用是 。
②步骤Ⅱ中用到的玻璃仪器除烧杯外还有 ;步骤Ⅳ中需要洗涤固体SnO中含有的杂质,检验SnO中的Cl-是否洗涤干净的操作为 。
③步骤Ⅴ涉及到的操作有:a.过滤 b.洗涤 c.蒸发浓缩 d.冷却结晶 e.低温干燥,则其正确的操作顺序为 。
(2)实验室拟用以下装置,用熔融的金属锡与干燥纯净的氯气制取无水SnCl4(SnCl4熔点-33℃,沸点114.1℃,遇潮湿空气极易水解),此反应过程放出大量的热。
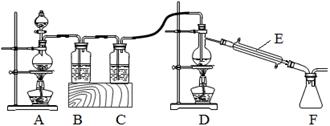
①装置C中应加入试剂为___________;仪器E的名称为____________________。
②反应开始生成SnCl4时,可以先熄灭___(填字母序号)处的酒精灯,理由是________。
③该实验装置设计尚存在缺陷,改进的方法是(包括仪器、试剂及连接位置等)______________。
(1)①防止Sn2+被氧化(2分) ②普通漏斗(或漏斗)、玻璃棒(2分);取最后一次洗涤液少许于试管中,滴加稀硝酸和AgNO3溶液,若无明显现象,证明SnO中的Cl-已洗涤干净;若产生白色沉淀证明SnO中的Cl-未洗涤干净(3分) ③cdabe(2分)
(2)①浓硫酸(2分);冷凝管(2分)
②D(2分);熔融的金属锡与氯气反应过程中放出大量的热,能维持该反应继续进行(2分)
③需要温度计;在装置F后应连接一个装有碱石灰(或氢氧化钠固体)的干燥管(或U型管)(2分)
题目分析:(1)①由于Sn2+易被氧化,所以SnCl2酸溶后加入Sn粉的作用是防止Sn2+被氧化。
②步骤Ⅱ中得到漏液B和滤渣,说明该操作是过滤,因此用到的玻璃仪器除烧杯外还有普通漏斗(或漏斗)、玻璃棒;氯离子的检验一般是用硝酸酸化的硝酸银溶液,所以检验SnO中的Cl-是否洗涤干净的操作为:取最后一次洗涤液少许于试管中,滴加稀硝酸和AgNO3溶液,若无明显现象,证明SnO中的Cl-已洗涤干净;若产生白色沉淀证明SnO中的Cl-未洗涤干净。
③从溶液中得到晶体的正确操作是蒸发浓缩、.冷却结晶、过滤、洗涤、低温干燥,因此正确的顺序是cdabe。
(2)①由于SnCl4熔点-33℃,沸点114.1℃,遇潮湿空气极易水解,因此通入的氯气必须是干燥的,则装置C中应加入试剂为浓硫酸;根据仪器的结构特点可知,仪器E的名称为冷凝管。
②由于熔融的金属锡与氯气反应过程中放出大量的热,能维持该反应继续进行,所以反应开始生成SnCl4时,可以先熄灭D处的酒精灯。
③反应需控制在一定温度范围之内,需要温度计;根据题意知SnCl4遇潮湿空气便发生水解反应,生成物应干燥,因此应在装置F后应连接一个装有碱石灰(或氢氧化钠固体)的干燥管(或U型管)可达到目的。
