(1)有A、B、C、D四种可溶性离子化合物,它们的阳离子是Ag+、Na+、Mg2+、Cu2+,阴离子是Cl-、OH-、NO3-、SO42-(每种离子只能用一次)现将溶液两两混合,记录现象如下:
A+B→白色沉淀B+D→白色沉淀C+D→蓝色沉淀
写出上述反应对应的离子方程式:
A+B→白色沉淀:______;
B+D→白色沉淀:______;
C+D→蓝色沉淀:______.
(2)向NaHSO4溶液中逐滴加入Ba(OH)2溶液至溶液呈中性,写出发生反应的离子方程式:______.
(1)用表格法进行分析,将溶液两两混合的现象结果记入右表,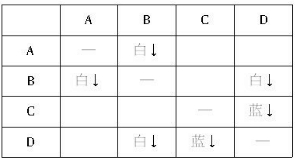
发现B与其他物质反应产生两种白色沉淀(肯定是不同的物质),而题设各离子中能组合为白色沉淀的物质有AgCl、Mg(OH)2;又D与其他物质反应产生一种白色沉淀、一种蓝色沉淀,题设各离子中能组合为蓝色沉淀的物质只有Cu(OH)2,这样可以确定D中含OH-,从而确定D为NaOH;再由“B+D→白色沉淀”确定B为MgCl2;由A、B反应情况确定A为AgNO3;由C、D反应情况确定C为CuSO4.故四种物质分别为AgNO3、MgCl2、CuSO4、NaOH,
AgNO3、MgCl反应的离子方程式为Ag++Cl-=AgCl↓;
MgCl2、NaOH反应的离子方程式为Mg2++2OH-=Mg(OH)2↓;
CuSO4、NaOH反应的离子方程式为Cu2++2OH-=Cu(OH)2↓,
故答案为:Ag++Cl-=AgCl↓;Mg2++2OH-=Mg(OH)2↓;Cu2++2OH-=Cu(OH)2↓;
(2)向NaHSO4 溶液中逐滴加入Ba(OH)2 溶液至溶液呈中性,SO42-过量,H+恰好反应,反应的离子方程式为2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O,
故答案为:2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O.
