二氧化钛(TiO2)广泛用于制造高级白色油漆,也是许多反应的催化剂.工业上用钛铁矿[主要成分为FeTiO3(钛酸亚铁,不溶于水)、Fe2O3及少量SiO2杂质]作原料,制取二氧化钛及绿矾,其生产流程如下:
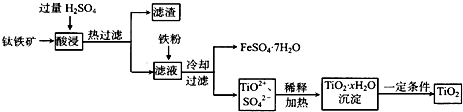
回答下列问题:
(1)Ti原子序数为22,则Ti位于周期表第______周期,第______列.
(2)FeTiO3溶于过量硫酸的离子方程式______.
(3)流程中生成TiO2•xH2O离子方程式为______.
(4)若铁粉的用量不足,可能导致产品TiO2中混有______杂质.
(5)以TiO2为原料制取金属钛的其中一步反应为TiO2+Cl2+C
TiCl4+______,已知该反应中氧化剂与还原剂的物质的量之比为1:1,则另一生成物为______. 高温 .
(6)TiCl4 在常温下呈液态,且极易水解,可以用作军事烟雾剂;写出其水解反应的方程式______.
(1)22-2-8-8=4,故Ti元素处于第四周期,第4列.
故答案为:四、4.
(2)由工艺流程转化关系可知,FeTiO3溶于过量硫酸,生成Fe2+、TiO2+、H2O,反应离子方程式为FeTiO3+4H+=Fe2++TiO2++2H2O.
故答案为:FeTiO3+4H+=Fe2++TiO2++2H2O.
(3)由工艺流程转化关系可知,TiO2+在加热条件下与水反应生成TiO2•xH2O,根据电荷守恒可知还生成H+,所以反应离子方程式为TiO2++(x+1)H2O=TiO2•xH2O+2H+.
故答案为:TiO2++(x+1)H2O=TiO2•xH2O+2H+.
(4)铁粉的用量不足,滤液中的Fe3+,不能除尽.生成的TiO2•xH2O沉淀中含有氢氧化铁,最后氢氧化铁分解生成氧化铁,所以可能导致产品TiO2中混有Fe2O3.
故答案为:Fe2O3.
(5)反应中Ti元素化合价未变化,氯元素化合价由0价降低为-1价,令碳元素在产物中等化合价为a,则a=2×[0-(-1)],故a=2,反应中氧化剂与还原剂的物质的量之比为1:1,结合元素守恒可知,TiO2、Cl2、C、TiCl4的系数分别为1、2、2、1,所以未知物中含有C原子与O原子,碳元素化合价为+2,故为CO,系数为2.
故答案为:2CO;CO.
(6)TiCl4 水解,生成H2TiO3与HCl,H2TiO3是固体颗粒,HCl与空气中水蒸气结合呈白雾,可以用作军事烟雾剂.水解方程式为TiCl4•+3H2O=H2TiO3+3HCl↑.
故答案为:TiCl4•+3H2O=H2TiO3+3HCl↑.
