根据要求完成下列各题实验目的.(a、b为弹簧夹,加热及固定装置已略去)
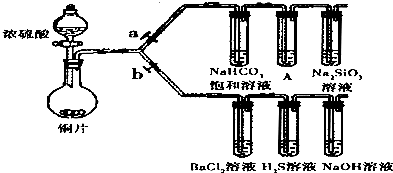
(1)验证碳、硅非金属性的相对强弱.
①实验操作:连接仪器、______、加入药品,打开a关闭b,滴入浓硫酸,加热.
②装置A中发生的化学方程式是______.
③能说明碳的非金属性比硅强的实验现象是:______.
(2)验证 SO2的氧化性、还原性和酸性氧化物的通性.
①H2S溶液中,其发生的离子方程式是______.
②将反应后的BaCl2溶液分成两份,第一份滴加氯水,第二份滴加氨水,则两份溶液中有何现象:______.
③验证SO2的还原性的离子方程式是______.
(1)①、装置A中反应制备气体,在加入药品之前需要检验装置的气密性,
故答案为:检验装置的气密性;
②、装置A的作用是除去二氧化硫,防止干扰二氧化碳与水硅酸钠的反应,可以利用强氧化性物质如:酸性高锰酸钾溶液,反应方程式为:5SO2+2KMnO4+2H2O=K2SO4+2MnSO4+2H2SO4,
故答案为:5SO2+2KMnO4+2H2O=K2SO4+2MnSO4+2H2SO4;
③、利用强酸制备弱酸,酸性越强,最高价氧化物水化物的酸性越强,中心元素的非金属性越强,A中KMnO4溶液没有完全褪色,盛有Na2SiO3溶液的试管中出现白色沉淀,说明碳的非金属性比硅强,
故答案为:A中KMnO4溶液没有完全褪色,盛有Na2SiO3溶液的试管中出现白色沉淀;
(2)①、H2S溶液中二氧化硫与硫化氢反应生成硫单质与水,反应离子方程式为:2H2S+SO2=3S↓+2H2O,
故答案为:2H2S+SO2=3S↓+2H2O;
②、应后的BaCl2溶液中含有亚硫酸,亚硫酸被氯水氧化物硫酸,硫酸与氯化钡反应生成硫酸钡,亚硫酸与氨水反应生成亚硫酸铵,亚硫酸铵与氯化钡反应生成硫酸钡,故都产生白色沉淀,
故答案为:两份溶液中均有白色沉淀生成;
③、二氧化硫被氯水氧化为硫酸,反应中二氧化硫表现还原性,同时与氯化钡反应生成硫酸钡沉淀,故反应离子方程式为:Ba2++SO2+Cl2+2H2O=BaSO4↓+4H++2Cl-,
故答案为:Ba2++SO2+Cl2+2H2O=BaSO4↓+4H++2Cl-.
