某化学研究性学习小组为了探究四氯化锡的有关性质,拟先利用下列装置和药品进行四氯化锡的制备.已知四氯化锡具有强的吸水性,SnCl4和Sn的部分数据如下
| 密度 | 熔点 | 沸点 | |
| 四氯化锡 | 2.2g•cm-3 | -33℃ | 114℃ |
| 金属锡 | 5.77g•cm-3 | 231℃ |
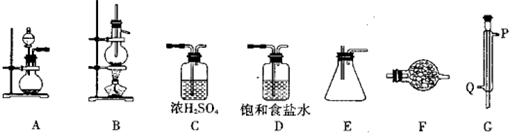
请回答下列相关问题:
(1)实验时装置的正确连接顺序为A→______→______→______→______→______→______;
(2)仪器G的名称是______;实验时,G中冷却水的流向是从______进入(填符号);
(3)A中发生反应的离子方程式为______;
(4)F中盛装的化学试剂是______;其作用是______;
(5)IVA族从上到下有C、Si、Ge、Sn、Pb等元素,请比较该族元素最高价氧化物对应水化物碱性的强弱顺序为(用化学式表示)______.
(1)用A制备氯气,分别在D、C中进行除杂和干燥,然后在B中发生反应制备SnCl4,冷却后在E中收集,最后连接F,进行尾气吸收,连接顺序为D→C→B→G→E→F,
故答案为:D→C→B→G→E→F;
(2)G为冷凝管,为达到充分冷凝的效果,应从Q进水,从P出水,故答案为:冷凝管;Q;
(3)A中制备氯气,在不加热的条件下进行,应用高锰酸钾和浓盐酸制备,反应的离子方程式为2MnO4-+16H++10Cl-=2Mn2++5Cl2↑+8H2O,
故答案为:2MnO4-+16H++10Cl-=2Mn2++5Cl2↑+8H2O;
(4)F中盛装碱石灰,具有碱性,可与水或酸性气体反应,防止空气中的水分进入装置E中,吸收多余的Cl2防止污染,
故答案为:碱石灰;防止空气中的水分进入装置E中,吸收多余的Cl2防止污染;
(5)金属性:Pb>Sn>Ge,元素的金属性越强,对应的最高价氧化物的水化物的碱性越强,则Pb(OH)4>Sn(OH)4>Ge(OH)4,
故答案为:Pb(OH)4>Sn(OH)4>Ge(OH)4.
