黄铜矿的主要成分是CuFeS2(硫元素一2价,铁元素+2价).是工业炼铜的主要原料.已知黄铜矿在空气中焙烧生成cu、FeS和S02,FeS+2Hcl=FeCl+H2S.H2S是一种剧毒气体.某科研小组设计以黄铜矿为原料涮取单质铜和氯化铁晶体(FeCl3•6H2O)的流程如下:
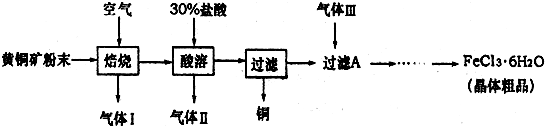
(1)92gCuFeS2在空气中焙烧生成Cu、FeS和S02转移电子的物质的量为______.
(2)请简述检验气体Ⅰ的操作步骤.
(3)在实验室中,欲用38%(密度为1.18g.mL-1)的盐酸配制30%的盐酸,需要的玻璃仪器主要有______.
(4)气体Ⅲ最好选用______(填写序号),其主要作用是______;
A.02 B.H2 C.Cl2 D.N2
欲选用下列仪器在实验室中制取纯净干燥的该气体.
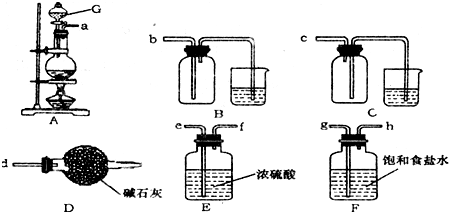
装置A中发生反应的离子方程式为______.
选用合适装置导管口的连接顺序为a接______.图中仪器G的名称是______;在使用该仪器时,应首先______.
(1)92gCuFeS2的物质的量=
=0.5mol,根据原子守恒可知生成Cu、FeS的物质的量分别为0.5mol、0.5mol,由硫原子守恒可知SO2的物质的量=0.5mol×2-0.5mol=0.5mol,反应中只有生成SO2的硫元素化合价升高,由-2价升高为+4价,故转移电子物质的量=0.5mol×[4-(-2)]=3mol,92g 184g/mol
故答案为:3mol;
(2)由工艺流程可知,焙烧产生的气体Ⅰ为SO2,利用品红溶液进行检验,具体操作为:收集适量气体Ⅰ通入品红溶液中,品红溶液褪色,加热溶液恢复红色,
故答案为:收集适量气体Ⅰ通入品红溶液中,品红溶液褪色,加热溶液恢复红色;
(3)用38%(密度为1.18g.mL-1)的盐酸配制30%的盐酸,用量筒量取需要浓盐酸与水的体积,在烧杯中稀释,丙用玻璃棒搅拌,故需要的仪器有:量筒、玻璃棒、烧杯,
故答案为:量筒、玻璃棒、烧杯;
(4)由工艺流程可知,过滤得到的滤液中主要为FeCl2,产品为FeCl3•6H2O,故通入的气体将Fe2+氧化为Fe3+,且不引入杂质,应为氯气最好;
制备干燥纯净的氯气:由发生装置可知,应是二氧化锰与浓盐酸加热制备,反应离子方程式为:MnO2+4H++2Cl-
Mn2++Cl2↑+2H2O; △ .
生成的氯气中含有HCl、水蒸气,利用饱和氯化钠溶液吸收氯气中的氯化氢气体;再利用浓硫酸除去氯气中的水蒸气,最后用氢氧化钠溶液吸收尾气中的氯气,连接时注意洗气与干燥装置导气管需要长进短出、收集装置应长进短出,故连接顺序为aghefb;
G是分液漏斗,使用之前应检查是否漏水,
故答案为:C;将Fe2+氧化为Fe3+;MnO2+4H++2Cl-
Mn2++Cl2↑+2H2O;ghefb;分液漏斗;检查是否漏水. △ .
