Na2O2可用作漂白剂和呼吸面具中的供氧剂.
(1)某学习小组发现:在盛有Na2O2的试管中加入足量水,立即产生大量气泡,当气泡消失后,向其中滴入1~2滴酚酞试液,溶液变红;将试管轻轻振荡,红色很快褪去;此时再向试管中加入少量MnO2粉末,又有气泡产生.
①使酚酞试液变红是因为______,红色褪去的可能原因是______.
②加MnO2粉末后发生的反应______.
写出Na2O2作供氧剂的反应方程式,并用双线桥表示电子转移的数目______.
(2)Na2O2有强氧化性,H2具有还原性,有同学猜想Na2O2与H2能反应.为了验证此猜想,该小组同学进行如下实验,实验步骤和现象如下.
步骤1:按图组装仪器(图中夹持仪器省略),检查气密性,装入药品;
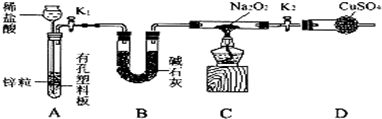
步骤2:打开K1、K2,产生的氢气流经装有Na2O2的硬质玻璃管,一段时间后,没有任何现象;
步骤3:检验H2的纯度后,开始加热,观察到硬质玻璃管内Na2O2开始熔化,淡黄色的粉末变成了白色固体,干燥管内硫酸铜未变蓝色;
步骤4:反应后撤去酒精灯,待硬质玻璃管冷却后关闭K1.
①盛装稀盐酸的仪器名称______;B装置的作用是______.
②必须检验氢气纯度的原因是______.
③设置装置D的目的是______.
④你得到的结论是______(若能反应请用化学方程式表示).
(1)①过氧化钠和水反应生成氢氧化钠是碱,碱遇酚酞变红;红色褪去的可能原因是过氧化钠和水反应生成的过氧化氢具有氧化性,能氧化有色物质,
故答案为:过氧化钠和水反应生成碱氢氧化钠;反应生成的H2O2具有漂白作用;
②过氧化氢在二氧化锰做催化剂分解生成水和氧气,反应的化学方程式为:2H2O2
2H2O+O2↑;在Na2O2与H2O反应生成了氢氧化钠和氧气,Na2O2与CO2反应生成了碳酸钠和氧气,在两个反应中,化合价升高数=化合价降低数=转移电子数=2,在Na2O2与H2O的反应生成了氢氧化钠和氧气,在Na2O2与H2O的反应中,化合价升高数=化合价降低数=转移电子数=2,电子转移情况为:MnO2 . 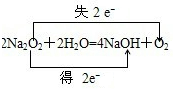 ,Na2O2与CO2反应生成了碳酸钠和氧气,在Na2O2与CO2的反应中,化合价升高数=化合价降低数=转移电子数=2,电子转移情况为:
,Na2O2与CO2反应生成了碳酸钠和氧气,在Na2O2与CO2的反应中,化合价升高数=化合价降低数=转移电子数=2,电子转移情况为: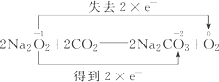 ;
;
故答案为:2H2O2
2H2O+O2↑;MnO2 .  、
、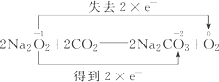 ;
;
(2)①分析装置图和实验步骤可知,盛盐酸的仪器为长颈漏斗;B装置是吸收氢气中的杂质气体,除去氢气中的水蒸气等,
故答案为:长颈漏斗;吸收氢气中的杂质气体;
②氢气是可燃性气体混有空气易点燃发生爆炸,验纯防止空气与氢气混合加热爆炸,
故答案为:防止空气与氢气混合加热爆炸;
③D装置是防止空气中的二氧化碳和水蒸气进入C影响实验验证,
故答案为:防止空气中的二氧化碳和水蒸气进入C装置和过氧化钠反应影响实验验证;
④实验现象分析可知过氧化钠变为白色固体,硫酸铜不变蓝色证明无水生成,证明氢气和过氧化钠反应生成氢氧化钠,反应的化学方程式为,Na2O2+H2
2NaOH,△ .
故答案为:氢气和过氧化钠反应生成氢氧化钠,Na2O2+H2
2NaOH.△ .
