电石浆是氯碱工业中的一种废弃物,其大致组成如表所示:
| 成分 | CaO | SiO2 | Al2O3 | Fe2O3 | MgO | CaS | 其他不溶于酸的物质 |
| 质量分数(%) | 65~66 | 3.5~5.0 | 1.5~3.5 | 0.2~0.8 | 0.2~1.1 | 1.0~1.8 | 23-26 |
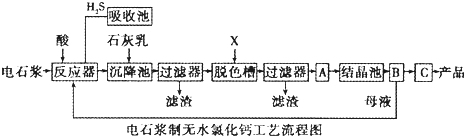
已知氯化钙晶体的化学式是:CaCl2•6H2O;H2S是一种酸性气体,且具有还原性.
(1)反应器中加入的酸应选用______.
(2)脱色槽中应加入的物质X是______;设备A的作用是______;设备B的名称为______;设备C的作用是______.
(3)为了满足环保要求,需将废气H2S通入吸收池,下列物质中最适合作为吸收剂的是______.反应的化学方程式为______.
A.水B.浓硫酸C.石灰乳D.硝酸
(4)将设备B中产生的母液重新引入反应器的目的是______.
(5)氯碱工业电极方程式______.
(1)因要生产CaCl2,过程中不引入新的杂质离子,所以应选用盐酸,故答案为:盐酸;
(2)活性炭具有吸附性,可以进行溶液脱水.A后是结晶池,故A应为蒸发浓缩;从B中有母液出来,故B为过滤器.B中得到晶体,所以需要脱水干燥,才能得到CaCl2产品,
故答案为:活性炭;蒸发浓缩;过滤器;脱水干燥;
(3)H2S为酸性气体,应用碱液吸收,故选石灰乳,反应的化学方程式为Ca(OH)2+H2S=CaS+2H2O,
故答案为:C;Ca(OH)2+H2S=CaS+2H2O;
(4)设备B中产生的母液含有氯化物,回收利用,可以降低废弃物排放量,提高经济效益,
故答案为:对母液回收利用,降低废弃物排放量,提高经济效益;
(5)氯碱工业中电解饱和食盐水,阳极是氯离子失电子生成氯气,电解反应为:2Cl--2e-=Cl2↑,阴极是氢离子得到电子生成氢气,电解反应为:2H++2e-=H2↑;
故答案为:阳极为2Cl--2e-=Cl2↑,阴极为2H++2e-=H2↑.
