问题
填空题
(10分)
氯化亚铜(CuCl)是白色粉末,不溶于水、乙醇,熔点422℃,沸点1366℃,在空气中迅速被氧化成绿色,常用作有机合成工业中的催化剂。以粗盐水(含Ca2+、Mg2+、SO2-4等杂质)。Cu、稀硫酸,SO2等为原料合成CuCl的工艺如下:
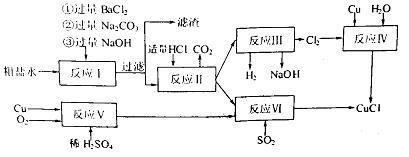
(1)反应I中加Na2CO3溶液的作用是 。
过一步反(2)反应II在电解条件下进行,电解时阳极发生的电极反应可表示为 。
(3)写出反应VI的化学方程式 。
(4)反应IV加入的Cu必须过量,其目的是 。
(5)反应VI后,过滤得到CuCl沉淀,用无水乙醇洗涤沉淀,在真空干燥机内于70℃干燥2小时,冷却,密封包装即得产品。于70℃真空干燥的目的是 。
答案
(1)除去Ca2+和过量的Ba2+
(2)2Cl—2e-=Cl2↑
(3)2CuSO4+2NaCl+SO2+2H2O=2CuCl↓+2NaHSO4+H2SO4
或2CuSO4+2NaCl+SO2+2H2O=2CuCl↓+Na2SO4+2H2SO4
(4)防止生成CuCl2
(5)加快乙醇和水的蒸发,防止CuCl被空气氧化
