II. 2 阅读理解 Leseverstndnis 2 Wie trainiert man sein Gehirn Je lter wir werden, um so unaufmerksamer speichern wir Informationen. Das Leben wird immer mehr zur Routine (老一套), da geht der gewohnte Alltag nur allzu leicht zum einen Ohr rein und zum anderen raus. Die riesige Menge von Gedanken, die uns stndig durch den Kopf gehen, durchdringt (穿过) nur noch das, was uns wirklich interessiert oder berührt. In Bestform ist das Gehirn überhaupt nur sehr kurz, gegen Ende der Schulzeit, mit 16, 18 Jahren. Niemals vorher und nachher wei ein Mensch so viel. Er hat alle nur mglichen Arten des Denkens, Kombinierens und Speicherns gelernt, danach geht es meistens stetig bergab. Vergesslichkeit ist ein Zeichen dafür, dass sich die Zellen im Gehirn langweilen. Sie werden zu wenig oder falsch benutzt. Das macht sie langsam und unbeweglich, und nur ein gezieltes Training kann sie wieder mobilisieren (行动起来). Man sollte niemals aufhren zu lernen,“ rt Professor Ratmann. Wer neugierig, kontaktfreudig und offen für Anregungen bleibt, hlt auch sein Gehirn funktionsfhig.“ Untersuchungen haben ergeben, dass schon nach fünf Tagen geistiger Unttigkeit der Intelligenzquotient (IQ, 智商) um durchschnittlich fünf Punkte abnimmt! Ein dreiwchiger reiner Faulenzerurlaub kann sogar 20 IQ-Punkte kosten. Wenigstens einmal am Tag sollte man sein Gehirn trainieren. Hier ein paar Jogging“-Mglichkeiten: – Lesen Sie morgens Ihre Zeitung so schnell und konzentriert wie mglich. Fassen Sie nach jedem Artikel detailgenau zusammen, was Sie davon behalten haben. – Lernen Sie eine neue Sprache. Das trainiert die Konzentration, die Merkfhigkeit und Denkschnelligkeit. – Rechnen Sie im Kopf. üben Sie das groe Einmaleins (大乘法表). – Kaufen Sie aus dem Gedchtnis“ ein, lassen Sie den Zettel in der Tasche. Die beste Zeit zum üben ist morgens, womglich noch vor dem Frühstück. Wichtig ist, schnell aus dem verschlafenen Zustand herauszukommen. Gehirn-Jogging macht hellwach, und damit ist der Geist optimal aufnahmebereit. Sogar die Stimmung hebt sich, und man brennt geradezu darauf, den Tag zu beginnen. A.Entscheiden Sie bitte, welche Erklrung zu der zitierten Textstelle passt!(21-25 Titel)B.Whlen Sie bitte die richtige Lsung aus!(26-30 Titel)
Die beste Lern- und Gedchtniszeit ist ________.
A.gegen Ende der Kinderzeit mit 6, 8 Jahren
B.gegen Ende der Schulzeit mit 16, 18 Jahren
C.gegen Ende der Lehrzeit mit 18, 22 Jahren
D.gegen Ende der Studienzeit mit 22, 27 Jahren
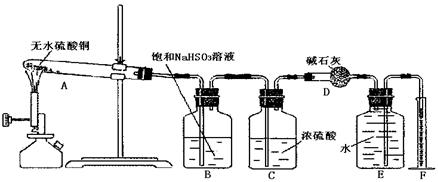
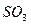 被
被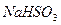 溶液吸收时产生了
溶液吸收时产生了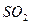 气体
气体 出氧气的体积为224mL(标准状况)。据此可计算出二氧化硫为 mol,三氧化硫为 mol。
出氧气的体积为224mL(标准状况)。据此可计算出二氧化硫为 mol,三氧化硫为 mol。