(6分)元素周期表是学习和研究化学的重要工具。请分析表中信息回答有关问题:
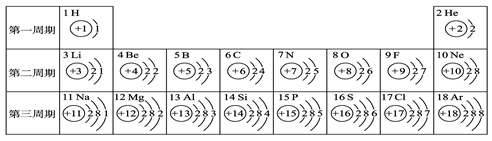
(1)表中 8号元素的一个原子在化学反应中易得到 个电子;表中最易失电子的元素形成的离子符号是 ;写出12号与17号元素组成的化合物的化学式 ;日本福岛核电站核泄漏中具有放射性的原子主要是碘-131,请根据右图推断碘在周期表中位于第 周期。
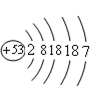
(2)分析表中信息,你能得出的规律是: 碘原子结构示意图
横行规律(任写一条)
纵行规律(任写一条)
⑴2 ; Na+ ;MgCl2;五(2)横行:自左而右,电子层数相同;或最外层电子数依次递增;或金属性逐渐减弱,非金属性逐渐增强。纵行:自上而下,最外层电子数相等;或电子层数依次增多;或金属性逐渐增强,非金属性逐渐减弱。
:(1)8号元素的最外层电子数是6个,要达到8电子稳定结构还差2个电子,所以在化学反应中易得到2个电子,最易失电子的元素是钠元素或氢元素、锂元素,最外层电子数是1个,12号元素是镁元素,易失去2个电子,化合价在化合物中显+2价,17号元素是氯元素,最外层电子数是7个,易得一个电子达稳定结构,化合价显-1价,依据化合价可写出化合物的化学式是MgCl2,碘元素原子核外有五个电子层,碘在周期表中位于第五周期;
故答案为:2;Na+(或H+Li+均可)MgCl2;五;
(2)通过元素周期表,可看出:同一周期中,原子序数从左向右逐渐递增,因为在原子中,原子序数=质子数=核外电子数,由此可知核外电子数从左向右逐渐递增,根据核外电子层的排布可知原子的核外电子层数相同,最外层电子数从左向右逐渐增多;观察纵行,可知:自上而下,最外层电子数相等(或电子层数依次增多).
故答案为:
同一周期中,原子的核外电子层数相同,或最外层电子数从左向右逐渐增多;
自上而下,最外层电子数相等(或电子层数依次增多).(合理皆可)
