问题
填空题
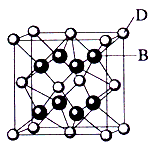
已知A、B、C、D和E都是元素周期表中前36号的元素,其原子序数依次增大。A与其他4种元素既不在同一周期又不在同一族。B和C属同一主族,D和E属同一周期,又知E是周期表中1-18列中的第8列元素。D的原子序数比E小6,D跟B可形成离子化合物其晶胞结构如图。 请回答
(1)写出B的电子排布图____________,C的元素符号是____________,B与A形成的化合物比C 与A形成的化合物沸点高,其原因是____________;
(2)E属元素周期表中第______周期,第______族的元素,其元素名称是____________,它的+2价离子的电子排布式为_____________________
(3)写出C的单质与水反应的化学方程式________________________;
(4)如图所示,D跟B形成的离子化合物的化学式为____________;鉴别该离子化合物是否为晶体,最可靠的科学方法是________________________,该离子化合物晶体的密度为ag·cm-3,B、D两元素的相对原子质量分别为b、c,则晶胞的体积是____________cm3(只要求列出算式)。
答案
(1)电子排布图:“略”;Cl;在氟化氢分子中存在氢键,分子间作用力大,破坏其作用力需要的温度较高,而氯化氢中不存在氢键,所以氟化氢的沸点高于氯化氢的沸点
(2)4;Ⅷ;铁;1s22s22p63s23p63d6
(3)Cl2+H2O==HCl+HClO
(4)CaF2;X射线衍射法;(8b+4c)/a NA
