(9分)
某合作学习小组分别利用装置Ⅰ、Ⅱ探究铜与硝酸的反应。
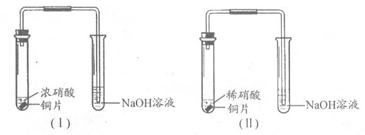
(1)Ⅰ中反应的离子方程式为 ;
Ⅱ中反应的化学方程式为 ;
比较装置Ⅰ、Ⅱ中的反应现象,其不同点是;
;
(2)该小组给Ⅰ反应后的溶液用小火加热一会儿,然后自然冷却。实验中观察到:试管上部气体颜色变深,并发现氢氧化钠溶液完全倒吸。倒吸后,试管中混合液呈淡蓝色,试管中有色气体消失。
①“试管上部气体颜色变深”的可能原因是 ;
②“倒吸”的原因是 ;
③“溶液呈淡蓝色”的可能原因是 。
(1)Cu+4H++2NO3- Cu2++2NO2↑+2H2O(2分)
3Cu+8HNO3 3Cu(NO3)2+2NO↑+4H2O(2分)
Cu在浓硝酸中反应剧烈,产生红棕色气体,溶液变为绿色;Cu在稀硝酸中反应,产生无色气体,遇空气后变红棕色,溶液变为蓝色。(2分)
(2)①硝酸受热分解产生NO2或2NO2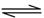 N2O4的平衡逆向移动(1分)
N2O4的平衡逆向移动(1分)
②氮的氧化物被NaOH溶液吸收,试管内压强降低(1分)
③NO2、硝酸与NaOH完全反应,溶液变为稀Cu(NO3)2溶液(1分)
