(16分)为测定碳酸钙纯度(设含杂质SiO2),学生设计了如下几个实验方案。请回答每个方案中提出的问题。
【方案I】
(1)称取碳酸钙样品M g;
(2)加入过量盐酸;
(3)收集并测定生成的气体体积V mL。
问题1:反应结束后,量气管中的显示如右图所示,接下来的操作是: ,读出甲管中液面的读数。
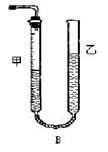
【方案II】
(1)称取碳酸钙样品M g;
(2)用c mol/L 盐酸V mL(过量)溶解样品;
(3)取溶解后的溶液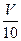 mL,以酚酞作指示剂,用c′ mol/L NaOH溶液滴定,恰好用去V′mL。
mL,以酚酞作指示剂,用c′ mol/L NaOH溶液滴定,恰好用去V′mL。
问题2:列出本实验中所用到的主要仪器名称(除铁架台及附件、烧杯之外) 。
问题3:碳酸钙纯度计算公式 。
问题4:当碳酸钙溶解完全后,少量未溶的SiO2没过滤去,结果得到碳酸钙纯度________ (偏大、偏小或无影响)
【方案Ⅲ】
(1)称取碳酸钙样品M g;
(2)加入足量c mol/L盐酸V mL使之完全溶解;
(3)过滤并取滤液;
(4)在滤液中加入过量c′ mol/L Na2CO3溶液V′mL;
(5)将步骤(4)中的沉淀滤出、洗涤、干燥、称重为M′g。
问题5:此方案中不需要的数据是 (填选项编号)。
A.c、V
B.c′、 V′
C. M′
D. M问题6:为减少实验误差,步骤(3)、(5)过滤后都要对沉淀进行洗涤,如果步骤(3)未经洗涤,则测定的碳酸钙的纯度将 (偏大、偏小、无影响,下同);如果步骤(5)未经洗涤,则测定的碳酸钙纯度将 。
问题7:判断步骤(4)中Na2CO3溶液是否过量的方法是 。
问题1:向下移动乙管,使甲、乙两管中的液面持平 (2分)
问题2:托盘天平、酸式滴定管(或移液管)、碱式滴定管、锥形瓶、药匙(4分)
问题3: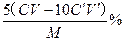 (3分)
(3分)
问题4:无影响 (1分)
问题5:A、B (2分)
问题6:偏小 偏大 (2分)
问题7:静置后,往上层清液中滴加Na2CO3溶液,若没有白色沉淀生成,则Na2CO3溶液过量 (2分)
