Mn、Fe均为第四周期过渡元素,两元素的部分电离能数据列于下表

回答下列问题:
(1)Mn元素价电子的电子排布式为___________________,比较两元素的I2、I3可知,气态Mn2+再失去一个电子比气态Fe2+再失去一个电子难。对此,你的解释是:___________________________
(2)Fe原子或离子外围有较多能量相近的空轨道能与一些分子或离子形成配合物。
①与Fe原子或离子形成配合物的分子或离子应具备的结构特征是____________________________
②六氯和亚铁离子〔Fe(CN)64-〕中的配体CN-中C原子的杂化轨道类型是_____________,写出一种与
CN-互为等电子体的单质分子的路易斯结构式___________________。
(3)三氯化铁常温下为固体,熔点:282℃,沸点315℃,在300℃以上升华。易溶于水,也易溶于乙醚、丙酮等有机溶剂。据此判断三氯化铁的晶体类型为:_______________
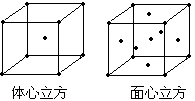
(4)金属铁的晶体在不同的温度下有两种堆积方式,晶体分别如图所示。面心立方晶胞和体心立方晶胞中实际含有的Fe原子个数之比为:____________
(1)3d54s2;由Mn2+转化为Mn3+时,3d能级由较稳定的3d5半充满状态转为不稳定的3d4状态需要的能量较多,而Fe2+到Fe3+时,3d能级由不稳定的3d6到稳定的3d5半充满状态,需要的能量相对要少
(2)①具有孤对电子;②sp;
(3)分子晶体
(4)2:1
