甲、乙两组同学在实验室分别完成以下任务:
甲组同学:将失去标签的两瓶无色溶液(分别为NaCl和Na2CO3)区别开来.
乙组同学:除去NaCl固体中的少量Na2CO3
(1)甲组同学为了区别两瓶无色溶液,A,B,C,D四位同学分别选择下列物质进行实验.其中合理的是______(填写序号).
A.稀盐酸
B.AgNO3溶液
C.澄清石灰水
D.酚酞
(2)乙组为了除去NaCl溶液中的少量Na2CO3,设计了如下的实验:
请回答下列问题:
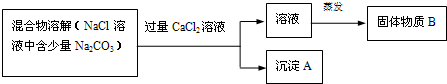
①写出沉淀A的化学式______;
②加入CaCl2溶液后,分离除去沉淀A的实验操作方法是______;
③上述方案很容易引入新的杂质.于是改进方案:将混合物溶解,若滴加盐酸至不再产生气体为止,则既能除去Na2CO3杂质,又能有效地防止新杂质的引入.写出有关反应的化学方程式______.
(1)鉴别NaCl和Na2CO3两种溶液,
A、稀盐酸能够和碳酸钠反应产生气泡,而与氯化钠混合无现象,故该方法合理;
B、AgNO3溶液和氯化钠、碳酸钠都会产生白色沉淀,故该方法不合理;
C、澄清石灰水能够和碳酸钠反应产生白色沉淀,而和氯化钠混合无现象,故该方法合理;
D、酚酞遇到碱性的碳酸钠溶液呈现红色,而遇到中性的氯化钠溶液不变色,故该方法合理;
故合理的是ACD;
(2)①Na2CO3与CaCl2溶液反应产生沉淀CaCO3,因此过滤得到的A是CaCO3;
②分离难溶性固体和液体使用过滤法;
③碳酸钠和盐酸反应产生氯化钠、水和二氧化碳,反应的方程式为:Na2CO3+2HCl═2NaCl+H2O+CO2↑.
故答案为:(1)ACD;(2)CaCO3;过滤;Na2CO3+2HCl═2NaCl+H2O+CO2↑.
