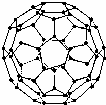
36、1996年诺贝化学奖授予对发现C60有重大贡献的三位科学家.C60分子是形如球状的多面体(如图),该结构的建立基于以下考虑:
①C60分子中每个碳原子只跟相邻的3个碳原子形成化学键;
②C60分子只含有五边形和六边形;
③多面体的顶点数、面数和棱边数的关系,遵循欧拉定理:顶点数+面数-棱边数=2
据上所述,可推知C60分子有12个五边形和20个六边形,C60分子所含的双键数为请回答下列问题:
(1)固体C60与金刚石相比较,熔点较高者应是______,理由是:______.
(2)试估计C60跟F2在一定条件下,能否发生反应生成C60F60(填“可能”或“不可能”)______,并简述其理由:______.
(3)通过计算,确定C60分子所含单键数. C60分子所含单键数为______.
(4)C70分子也已制得,它的分子结构模型可以与C60同样考虑而推知.通过计算确定C70分子中五边形和六边形的数目.
C70分子中所含五边形数为______,六边形数为______.
解(1)金刚石属原子晶体,是空间立体网状结构;C60是分子晶体,为足球结构,所以金刚石的熔点大于C60.
故答案为:金刚石;金刚石属原子晶体,而固体C60不是,故金刚石熔点较高.
(2)该分子中含有碳碳单键和双键,双键能发生加成反应,所以可能.
故答案为:可能;因C60分子含30个双键,与极活泼的F2发生加成反应即可生成C60F60 .
(3)由欧拉定理计算键数(即棱边数):60+(12+20)-2=90
该分子中含双键30个,所以单键数为:C60分子中单键为:90-30=60
(4)设C70分子中五边形数为x,六边形数为y.依题意可得方程组:
(5x+6y)=1 2
(3×70)1 2 70+(x+y)-
(3×70)=21 2
得x=12 y=25
故答案为:12;25.
