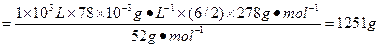问题
填空题
六价铬对人体有毒,含铬废水要经过化学处理后才能排放,方法是用绿矾(FeSO4·7H2O)把废水中六价铬还原成三价铬离子,再加入过量的石灰水,使铬离子生成Cr(OH)3沉淀。
(1)配平下列主要反应的化学方程式。
 H2Cr2O7+
H2Cr2O7+ FeSO4+
FeSO4+ H2SO4——
H2SO4—— Fe2(SO4)3+
Fe2(SO4)3+ Cr2(SO4)3+
Cr2(SO4)3+ H2O
H2O
(2)处理后的沉淀中有Cr(OH)3外,还有__________________ (用化学式表示)。
(3)现在处理1×103 L含铬(+6)78 mg·L-1的废水,需要绿矾_________ g。
答案
(1)1 6 6 3 1 7 (2)Fe(OH)3 (3)1 251
本题考查了氧化还原反应方程式的配平和计算。铬元素的化合价由+6降到+3,铁元素的化合价由+2升高到+3,应用得失电子守恒时要特别注意每个H2Cr2O7含有两个铬原子,再应用观察法配平整个化学方程式。
由H2Cr2O7+6FeSO4+6H2SO4====3Fe2(SO4)3+Cr2(SO4)3+7H2O可知:
2Cr—H2Cr2O7—6FeSO4·7H2O
m(FeSO4·7H2O)