问题
实验题
(9分)、已知FeSO4在不同条件下分解得到的产物不同,可能是FeO和SO3,也可能是Fe2O3、SO3和SO2。某研究小组探究在酒精喷灯加热条件下FeSO4分解的气体产物。已知SO3的熔点是16.8℃,沸点是44.8℃
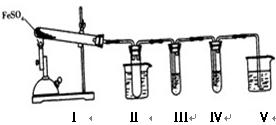
⑴装置Ⅱ的试管中不装任何试剂,其作用是 。试管浸泡在50℃的水浴中,目的是 。
| 检验试剂 | 预期现象与结论 |
| 装置Ⅲ的试管中加入 。 | 产生大量白色沉淀,证明气体产物中含有SO3 |
| 装置Ⅳ的试管中加入 。 | |
 Ⅳ的作用是探究本实验气体产物成分。请完成实验设计,填写检验试剂、预期现象与结论。限选试剂:3mol·L-1H2SO4、6 mol·L-1NaOH、0.5 mol·L-1BaCl2、0.5 mol·
Ⅳ的作用是探究本实验气体产物成分。请完成实验设计,填写检验试剂、预期现象与结论。限选试剂:3mol·L-1H2SO4、6 mol·L-1NaOH、0.5 mol·L-1BaCl2、0.5 mol· L-1Ba(NO3)2、0.01 mol·L-1酸性KMnO4溶液、0.01 mol·L-1溴水
L-1Ba(NO3)2、0.01 mol·L-1酸性KMnO4溶液、0.01 mol·L-1溴水⑶装置Ⅴ的作用是防止尾气污染环境,烧杯中应加入的试剂是 。
答案
(9分)、⑴防止溶液倒吸(或安全瓶)(2分);防止SO3液化或凝固(2分)
⑵
| 检验试剂 | 预期现象与结论 |
0. 5mol·L-1BaCl2溶液 5mol·L-1BaCl2溶液(1分) | 产生大量白色沉淀,证明气体产物中含有SO3 |
| 0.01 mol·L-1酸性KMnO4溶液 (或0.01 mol·L-1的溴水)(1分) | 若溶液的紫色(或橙色)褪去,证明气体产物中含有SO2。 若溶液中紫色(或橙色)无明显变化,证明气体产物中不含SO2。 (2分) |
⑶ NaOH溶液(1分)

