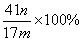(14分)氮化铝是一种新型的无机非金属材料,被广泛应用于集成电路生产领域。在氮气流中由氧化铝与焦炭在电炉中加热制得。原料配比不当或反应不完全等因素都会造成产品中含有碳、Al4C3或Al2O3等杂质。回答下列问题:
(1)反应Al2O3+N2+ 3C  2AlN+3CO中,氧化剂是 。
2AlN+3CO中,氧化剂是 。
(2)AlN也可以与强碱溶液反应。完成下列方程式:
AlN+NaOH+H2O= +
(3)Al 4C3与水反应生成甲烷,反应方程式是
甲烷与CuO反应的化学方程式如下:
CH4+4CuO  CO2+2H2O+4Cu
CO2+2H2O+4Cu
为测定产品中有关成分的含量,所需仪器如下:
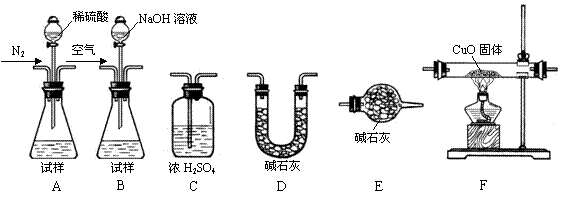 Ⅰ.测定样品中含有少量Al4C3的含量,各装置连接
Ⅰ.测定样品中含有少量Al4C3的含量,各装置连接 的顺序为A→C→F→C→D→E。主要实验步骤
的顺序为A→C→F→C→D→E。主要实验步骤 如下:
如下:
①称量D的质量,按顺序组装仪器,将试样放入锥形瓶中,检查装置的气密性
②从分液漏斗缓缓滴入稀硫酸,直到不再产生气体时为止
③点燃F酒精灯
④缓缓鼓入一定量的N2
⑤再次缓缓鼓入一定量的N2
⑥再次称量D的质量
⑦重复步骤⑤和⑥的操作,直到D的质量基本不变
操作的先后顺序是①→ →⑤→⑥→⑦,操作④的目的是  。
。
Ⅱ.为测定AlN的含量,请选择合适的药品和装置,按气流方向连接各装置,其顺序为:
→ → →E
若试样为mg,测得C增重n g,则AlN的质量分数是 。
(14分)(1)N2
(2)NaAlO2、NH3
(3)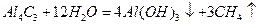
Ⅰ.④→③→②
将装置中的空气排尽,防止爆炸
Ⅱ. B→D→C