(10分)某同学用如图一所示装置来探究CO2、SO2与澄清石灰水的反应,结果通入CO2可以看到先浑浊后澄清的现象,但通入SO2没有看到浑浊现象。经过思考分析后,该同学改用图二的装置,将气体收集在注射器,缓缓地将气体一个气泡一个气泡地通入澄清石灰水中,都能看到石灰水先变浑浊再澄清的现象。

(1)SO2是空气污染物之一,它的危害是 。
(2)图一中生成CO2反应的离子方程式为 ;
(3)如何鉴别CO2和SO2(只需要写出一种方法,应写出操作方法、现象和结论)? 。
(4)用图一进行SO2与石灰水反应的实验时,从环保角度考虑,还需要增加什么装置,在方框中画出。
(5)对比分析两组实验,你认为用图一装置实验时,通过SO2不能出现浑浊的原因可能是 。
(1)会形成酸雨 (2)CO32-+2H+=H2O+CO2↑
(3)将两种气体分别通入品红溶液,褪色的是SO2,不褪色的是CO2
(4)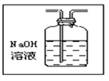 (“长进短出”为1分,“NaOH溶液”为1分)
(“长进短出”为1分,“NaOH溶液”为1分)
(5)SO2溶解度大,图一中SO2与石灰水反应时SO2过量,直接生成了酸式盐,因而看不到沉淀。
(1)SO2的危害主要是形成酸雨。
(2)硫酸的酸性强于碳酸的,所以硫酸和碳酸钠反应生成CO2气体,离子方程式为CO32-+2H+=H2O+CO2↑。
(3)SO2具有漂泊性,据此可以鉴别SO2和CO2。
(4)SO2有毒,所以必须有尾气处理装置,可以利用氢氧化钠溶液吸收剩余的SO2。
(5)由于SO2易溶于水,因此反应中SO2是过量的,生成的盐是酸式盐,看不到沉淀。
