利用中和反应可以测定酸或碱溶液中溶质的质量分数。例如,在一定量的待测酸(或碱)溶液中逐滴滴入已知质量分数的碱(或酸)溶液(这种溶液被称为标准溶液),直到酸、碱恰好完全反应,根据消耗标准碱(或酸)溶液的多少即可求算出待测酸(或碱)溶液的溶质质量分数。下图为某次测定过程中,溶液的pH随所滴加的某标准溶液体积的变化而变化的关系图。
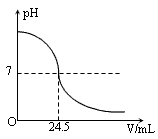
(1)根据上图曲线可以判断在实验中是向 (填“酸”或“碱”,下同)溶液(待测液)中滴加 溶液(标准液)。
(2)在这次测定中,为了指示中和反应刚好完全,用酚酞做指示剂,即在待测溶液中先滴入几滴酚酞试液,若看到 现象,则证明中和反应刚好完全。
(3)如果实验中使用的酸是硫酸溶液,碱是氢氧化钠溶液,且待测液和标准液的密度均以1.0g/mL计。若测定中取用待测液25mL,标准液溶质的质量分数为4.5%,根据图中数据,计算待测液溶质的质量分数。