(10分)乙二酸俗名草酸,某化学学习小组的同学欲探究测定草酸晶体(H2C2O4·xH2O)中x值。通过查阅资料该小组同学通过网络查询得,草酸易溶于水,水溶液可以用酸性KMnO4溶液进行滴定:
2MnO4-+5H2C2O4+6H+ 2Mn2++10CO2↑+8H2O
该组同学设计了滴定的方法测定x值。
①称取1.260 g纯草酸晶体,将其酸制成100.00 mL水溶液为待测液。
②取25.00 mL待测液放入锥形瓶中,再加入适量的稀H2SO4
③用浓度为0.1000 mol/L的KMnO4标准溶液进行滴定,达到终点时消耗10.00 mL;
请回答:
⑴滴定时,将KMnO4标准液装在下图中的 (填“甲”或“乙”)滴定管中。
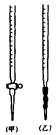
⑵本实验滴定达到终点的标志是
⑶通过上述数据,计算出x= 。
讨论:①若滴定终点时俯视滴定管刻度,则由此测得的x值会 (填“偏大”、“偏小”或“不变”,下同)。
②若滴定时所用的KMnO4溶液因久置而导致浓度变小,则由此测得的x值会
(10分)[每空2分](1)甲(2)最后一滴高锰酸钾滴入溶液突然出现紫色(或紫红色),且半分钟内不褪色(3)2 ①偏大 ②偏小)
(1)KMnO4溶液具有强氧化性,可腐蚀橡胶管,故只能用酸式滴定管甲
(2)由于KMnO4溶液本身为紫色,故不需要使用指示剂,当最后一滴高锰酸钾滴入溶液突然出现紫红色,且半分钟内不褪色,即为终点
(3)由2MnO4-~5H2C2O4可知,n(KMnO4)=0.001mol,待测液中n(H2C2O4)=0.0025mol,晶体中所含H2C2O4为0.01mol;晶体所含结晶水的物质的量为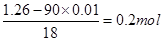 ,故晶体中n(H2C2O4):n(H2O)=1:2,故x=2
,故晶体中n(H2C2O4):n(H2O)=1:2,故x=2
①若滴定终点时俯视滴定管刻度,将导致标准液的体积偏小,所计算出的H2C2O4的量偏小,水的量偏大,则由此测得的x值会偏大
②若滴定时所用的KMnO4溶液因久置而导致浓度变小,将导致标准液的体积偏大,所计算出的H2C2O4的量偏大,水的量偏小,则由此测得的x值会偏小
