(15分)某化学研究小组探究无水三草酸合铁酸钾K3[Fe(C2O4)3]受热分解的产物,并对所得气体产物和固体产物进行验证,按下图装置进行实验(夹持仪器已略去)。
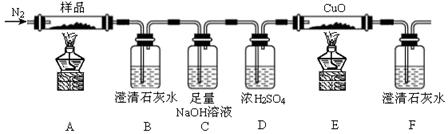
(1)连接好装置后,加入药品前,应该进行的实验操作是________________(填操作名称)。
(2)实验开始时缓缓通入氮气,过一段时间以后,加热反应管A和E ,待反应完全后,停止加热,仍继续通氮气,直到反应管冷却。停止加热前是否需要先断开A、B的连接处和E、F的连接处?为什么?_______________________________________________________________。
(3)实验中观察到B中澄清石灰水变浑浊,则说明气体产物中有 (写化学式)。
能证明分解产物中有CO气体生成的实验现象是 。
(4)该小组同学查阅资料后得知,固体产物中不存在+3价Fe元素,而盐类物质只有K2CO3。
① 验证固体产物中钾元素存在的方法是 ,现象是 。
② 研究小组为探究铁元素的存在形式,取A中充分反应后所得固体于试管中,加入足量蒸馏水,过滤、洗涤、干燥得到黑色粉末,取4.4g黑色粉末溶于足量稀硝酸中,收集到标准状况下NO气体1.12L通过计算判断黑色粉末的成分为 (写化学式)。写出黑色粉末溶于足量稀硝酸发生反应的离子方程式 。
(1)检查装置的气密性(1分)
(2)不需要(1分) 因为N2不断通入,B、F瓶溶液不会倒吸。(1分)
(3)CO2(1分) E中黑色固体变成红色,F中溶液变浑浊(2分)
(4)①焰色反应(2分) 透过蓝色的钴玻璃观察到紫色火焰(1分)
②FeO 和Fe 3FeO +10H+ +NO3-=3Fe3++NO↑+5H2O
Fe+4H+ +NO3-=Fe3++NO↑+2H2O (每空2分)
(1)连接好装置后,加入药品前,应该进行的实验操作是必须检验装置的气密性。
(2)由于氮气持续的不断通入,而氮气是不溶于水的,所以不会造成溶液的倒吸,因此没有必要断开A、B的连接处和E、F的连接处。
(3)因为CO2能使澄清的石灰水变混浊,所以如果实验中观察到B中澄清石灰水变浑浊,则说明气体产物中有CO2。CO具有还原性,能把氧化铜还原生成红色的铜,而CO则被氧化生成CO2,CO2能使澄清的石灰水变混浊,据此可以判断。
(4)①检验钾元素常用焰色反应,但观察钾元素的焰色反应需要透过蓝色的钴玻璃观察。
②NO的物质的量是0.05mol,则转移电子是0.05mol×3=0.15mol。如果是铁,则铁是0.05mol,
质量是0.05mol×56g/mol=2.8g。如果是氧化亚铁,则其物质的量是0.15mol,质量是0.15mol
×72g/mol=10.8g。由于物质总共是4.4g,所以应该是FeO 和Fe的混合物。和硝酸反应的方程
式为3FeO +10H+ +NO3-=3Fe3++NO↑+5H2O、Fe+4H+ +NO3-=Fe3++NO↑+2H2O。
