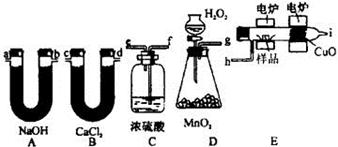
(共10分)化学上常用燃烧法确定有机物的组成.这种方法是在电炉加热时用纯氧气氧化管内样品,根据产物的质量确定有机物的组成.下图所列装置是用燃烧法确定有机物分子式常用的装置.
回答下列问题:
(1)产生的氧气按从左到右流向,所选装置各导管的连接序号(填写接口代号)是:
________________________________________;
(2)C装置中浓H2SO4的作用是________________________________;
(3)D装置中MnO2的作用是__________________________________;
(4)燃烧管中CuO的作用是___________________________________;
(5)若准确称取 0.90 g样品(只含 C、H、O三种元素中的两种或三种),经充分燃烧后,
A管质量增加1.32 g,B管质量增加0.54 g,则该有机物所含元素的最简比为___________。
(1)g、f、e、h、i、c、d、a、b;(2)吸收水分,得干燥纯净的O2 (3)催化剂(4)使有机物充分氧化成CO2和H2O (5)CH2O
考查有机物分子式的确定。
D装置是生成氧气的,利用二氧化锰的催化作用使双氧水分解产生氧气。由于参与反应的氧气必须是纯净干燥的,所以需要对生成的氧气进行净化处理,用浓硫酸干燥氧气,然后和有机物反应。有机物的燃烧产物首先应该是用无水氯化钙来吸收生成的水,然后再用氢氧化钠吸收生成的CO2;有机物在燃烧过程中也可能燃烧不充分,从而生成CO,因此需要用氧化铜来氧化可能生成的CO;A管质量增加1.32 g,则CO2的质量是1.32g,物质的量是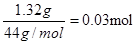 。B管质量增加0.54 g,则水是0.54g,物质的量是
。B管质量增加0.54 g,则水是0.54g,物质的量是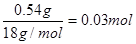 。所以有机物中氧原子的质量是0.90g-0.03mol×12g/mol-0.06mol×1g/mol=0.48mol,物质的量是0.03mol,所以C、H、O的个数之比是1︰2︰1,因此最简式是CH2O。
。所以有机物中氧原子的质量是0.90g-0.03mol×12g/mol-0.06mol×1g/mol=0.48mol,物质的量是0.03mol,所以C、H、O的个数之比是1︰2︰1,因此最简式是CH2O。
