(9分)下列是与硫元素相关的一系列实验:根据下图所示实验回答下列问题:

(1)试管A中发生的化学反应方程式是 。
(2)反应一段时间后,停止反应,将B试管中的溶液加热,可以观察到 。试管C中溶液变浑浊,则证明SO2具有 性。
(3)试管C口部的棉团既可浸碱溶液,又可浸NaHCO3溶液,其作用是 ,如果浸NaHCO3溶液,则发生反应的化学方程式是 。
(4)如将B试管换成D试管,并从直立导管中向BaCl2溶液中通入另一种气体,产生白色沉淀,则气体可以是
(5)如果反应过程中要立即停止反应,最简单的方法是 。
(1)Cu+2H2SO4 (浓)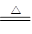 CuSO4+SO2↑+2H2O(2分)
CuSO4+SO2↑+2H2O(2分)
(2) 溶液由无色变成红色;(1分)氧化性(1分)
(3)吸收尾气,防止环境污染;(1分) SO2+NaHCO3=NaHSO3+CO2 (2分)
(4)NH3、NO2、Cl2、ClO2、O3中的一种,其他合理答案即可(1分)
(5)抽出铜丝到液面上(1分)
浓硫酸具有强氧化性,在加热的条件下与铜发生氧化还原反应,方程式为:Cu+
2H2SO4 (浓)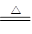 CuSO4+SO2↑+2H2O;产物SO2具有漂泊性可与有色物质化合生成不稳定的无色物质,因此能使品红溶液褪色,但在加热的情况下无色物质会恢复原来的颜色,所以将B试管中的溶液加热后,品红会恢复红色;H2S具有还原性可被SO2氧化生成单质硫,方程式为:2H2S+SO2=3S+2H2O;SO2属于大气污染物,需要进行尾气处理;SO2与BaCl2溶液不反应,要想生成白色沉淀,必须把SO2氧化成硫酸,然后产生BaSO4沉淀,或者降低溶液的酸性产生BaSO3沉淀;由于铜丝是活动的,因此要立即停止反应,最简单的方法是抽出铜丝和液面脱离。
CuSO4+SO2↑+2H2O;产物SO2具有漂泊性可与有色物质化合生成不稳定的无色物质,因此能使品红溶液褪色,但在加热的情况下无色物质会恢复原来的颜色,所以将B试管中的溶液加热后,品红会恢复红色;H2S具有还原性可被SO2氧化生成单质硫,方程式为:2H2S+SO2=3S+2H2O;SO2属于大气污染物,需要进行尾气处理;SO2与BaCl2溶液不反应,要想生成白色沉淀,必须把SO2氧化成硫酸,然后产生BaSO4沉淀,或者降低溶液的酸性产生BaSO3沉淀;由于铜丝是活动的,因此要立即停止反应,最简单的方法是抽出铜丝和液面脱离。
