问题
填空题
决定物质性质的重要因素是物质结构。请回答下列问题。
(1)已知A和B为第三周期元素,其原子的第一至第四电离能如下表所示:
| 电离能/kJ·mol-1 | I1 | I2 | I3 | I4 |
| A | 578 | 1817 | 2745 | 11578 |
| B | 738 | 1451 | 7733 | 10540 |
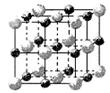
(2)实验证明:KCl、MgO、CaO、TiN这4种晶体的结构与NaCl晶体结构相似(如上图所示),其中3种离子晶体的晶格能数据如下表:
| 离子晶体 | NaCl | KCl | CaO |
| 晶格能/kJ·mol-1 | 786 | 715 | 3401 |
(3)金属阳离子含未成对电子越多,则磁性越大,磁记录性能越好。离子型氧化物V2O5和CrO2中,适合作录音带磁粉原料的是 。
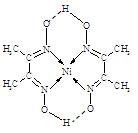
(4)某配合物的分子结构如上图所示,则N原子的杂化方式为 ;基态Ni原子的电子排布式 。
答案
(1)>(2分)
(2)TiN>MgO>CaO>KCl(2分,有1项排错即给0分) 12(2分)
(3)CrO2(2分)
(4)sp2(2分) [Ar]3d74s2(2分)
