(11分)以下是某学习小组对乙二酸的某些性质进行研究性学习的过程:
[研究课题]探究乙二酸的某些性质
[查阅资料]乙二酸(HOOC-COOH)俗称草酸,其主要物理常数如下:
| 名称 | 乙二酸 | 乙二酸晶体 |
| 分子式 | H2C2O4 | H2C2O4·2H2O |
| 颜色状态 | 无色固体 | 无色晶体 |
| 溶解度(g) | 8.6(20℃) | — |
| 熔点(℃) | 189.5 | 101.5 |
| 密度(g·cm-3) | 1.900 | 1.650 |
草酸在100℃时开始升华,157℃时大量升华,并开始分解。
草酸钙不溶于水。
草酸蒸气能使澄清石灰水变浑浊。
草酸蒸气在低温下可冷凝为固体。
根据上述材料提供的信息,回答下列问题:
[提出猜想]
(猜想一)根据草酸晶体的组成对其分解产物进行猜想
设计方案:
(1)该小组同学猜想其产物为CO、CO2和H2O,请用下列装置组成一套探究实验装置(草酸晶体分解装置略,装置可重复使用,连接导管略去)。
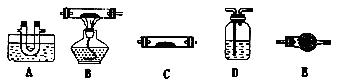
A中水槽装冰水混合物、B中装氧化铜、C中装无水硫酸铜,D中装澄清石灰水、E中装碱石灰
请回答下列问题:
①装置的连接顺序为:A→_____________________________________________。
②检验产物中CO的实验现象是____________________________________________________________
③整套装置是否存在不合理之处, (填是或否),若有该如何解决___________________________________________________________________________
(猜想二)乙二酸具有弱酸性
设计方案:
(2)该小组同学为验证草酸具有弱酸性设计了下列实验,其中能达到实验目的是______(填字母)。
A.将草酸晶体溶于含酚酞的NaOH溶液中,溶液褪色
B.测定相同浓度的草酸和硫酸溶液的pH
C.测定草酸钠(Na2C2O4)溶液的pH
D.将草酸溶液加入Na2CO3溶液中,有CO2放出
(猜想三)乙二酸具有还原性
设计方案:
(3)该小组同学向用硫酸酸化的KMnO4溶液中滴入过量的草酸溶液,发现酸性KMnO4溶液褪色,从而判断草酸具有较强的还原性。配平该反应的离子方程式:
___MnO4-+___H2C2O4 +___H+ ===___Mn2+ +___CO2↑+___H2O
(4)利用上述原理可定量测定某草酸晶体样品(含有H2C2O4·2H2O及其它一些杂质)中H2C2O4·2H2O的含量。
方法是:称取该样品0.12 g,加适量水完全溶解,然后用0.020 mol·L-1
的酸性KMnO4溶液滴定至终点(杂质不参与反应),滴定前后滴定管中的液面读数如图所示(单位:mL),则该草酸晶体样品中H2C2O4·2H2O的质量分数为_____________。
(已知相对原子质量:Mr(H2C2O4·2H2O)=126)
(11分)(1)①A→C→D→E→B→D(2分)
②黑色固体变成红色,且澄清石灰水变浑浊(1分)
③是(1分) 无尾气处理装置,将尾气通到燃着的的酒精灯上(1分)(其它合理答案也给分)
(2)BC(2分,多选倒扣,扣完为止)
(3)2,5,6="2,10,8" (2分) (4)84.0%(2分)
(1)①由于草酸蒸气能使澄清石灰水变浑浊,而草酸蒸气在低温下可冷凝为固体,所以要先把草酸蒸汽冷却变成固体。无水硫酸铜用来检验水蒸气,澄清的石灰水用来检验CO2,氧化铜用来检验CO。由于通过溶液必然会带出水蒸气,所以首先检验水蒸气。由于CO的氧化产物也是CO2,所以要先检验CO2,最后检验CO。和氧化铜反应的CO应该是干燥的,所以需要进行干燥处理,因此正确的顺序为A→C→D→E→B→D
② CO能把氧化铜还原生成红色的单质铜,而CO被液化生成CO2,所以检验产物中CO的实验现象是黑色固体变成红色,且澄清石灰水变浑浊。
③由于CO是有毒气体,所以需要增加尾气处理装置,即将尾气通到燃着的的酒精灯上,使其燃烧。
(2)A、D都只能说明乙二酸显酸性,但不能证明存在电离平衡。所以BC是正确的,弱酸的导电性小于相同条件下的强酸的导电性。弱酸盐存在水解平衡,答案选BC。
(3)根据氧化还原反应中电子的得失守恒进行配平。KMnO4是氧化剂,反应中锰的化合价从+7价降到+2价,得到5个电子。H2C2O4是还原剂,碳元素的化合价由+3价,升高到+4价,1mol还原剂失去2mol电子,所以氧化剂和还原剂的物质的量之比是2︰5,即方程式为2MnO4-+5H2C2O4 +6H+=2Mn2+ +10CO2↑+8H2O。
(4)根据滴定管中的读数可知,消耗酸性KMnO4溶液的体积是18.50ml-2.50mol=16.00ml。所以消耗酸性KMnO4的物质的量是0.020mol/L×0.016L=0.00032mol,则消耗乙二酸是0.00032mol÷2×5=0.0008mol,其质量是0.0008mol×126g/mol=0.1008g,所以其质量分数为0.1008÷0.12×100%=84.0%
