问题
填空题
(8分)某烧碱溶液中含有少量杂质(不与盐酸反应),现用中和滴定测定其浓度。
(1)滴定
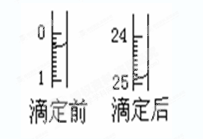
①用______式滴定管盛装0.1000 mol/L盐酸标准 液,锥形瓶中装有25.00mL待测烧碱溶液。上图表示某次滴定时50 mL滴定管中前后液面的位置。请将用去的标准盐酸的体积填入②表空格中。
②有关数据记录如下:
| 滴定序号 | 待测液体积(mL) | 所消耗盐酸标准液的体积(mL) | ||
| 滴定前 | 滴定后 | 消耗的体积 | ||
| 1 | 25.00 | 0.50 | 25.95 | 25.45 |
| 2 | 25.00 | 0.30、 | ||
| 3 | 25.00 | 6.00 | 31.55 | 25.55 |
c(NaOH) = _____________ 。
(3)读数时,若滴定前仰视,滴定后俯视,则会使最终测定结果_________。(填“无影响”、“偏高”、“偏低”)
答案
(1)酸式(1分) 0.3 24.90、24.60 (各1分) (2)0.1020mol/L (3)偏低
(1)①盐酸显酸性,应该用酸式滴定管盛放。
②根据滴定管中液面可知,此时读数是24.90ml,所以稀释盐酸是24.60ml。
(2)根据消耗的盐酸溶液体积可知,实验2中数据误差太大,属于是无效的。所以实验1、3中消耗的平均值是25.50ml,因此氢氧化钠的物质的量浓度是

(3)滴定前仰视,则读数偏大。滴定后俯视,则读数偏小,所以消耗的盐酸体积偏小,浓度偏低。
