(8分)某小组取一定质量的FeSO4固体,利用下图装置进行实验。
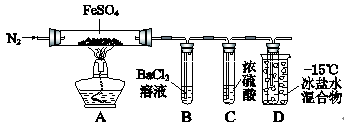
| 实验过程 | 实验现象 | |
| ① | 通入一段时间N2,加热 | A中固体变为红棕色,B中有白色沉淀,D试管中有无色液体 |
| ② | 用带有火星的木条靠近装置D的导管口 | 木条复燃 |
| ③ | 充分反应,停止加热,冷却后,取A中固体,加盐酸 | 固体溶解,溶液呈黄色 |
| ④ | 将③所得溶液滴入D试管中 | 溶液变为浅绿色 |
(1)实验③反应的离子方程式是_______。
(2)分解过程除产生使木条复燃的气体外,仅由A中固体颜色变化推测,还一定有______气体,依据是_______。
(3)实验④反应的离子方程式是_______。
(4)某同学依据B中的现象,认为FeSO4分解一定有SO3生成。你认为是否正确,原因是(用必要的文字和化学方程式解释)_______。
(1)Fe2O3+6H+=2Fe3++3H2O (2)SO2 因为有Fe2O3生成,在FeSO4中只有+6价S元素有氧化性,能被还原。因此一定有SO2生成。
(3)2Fe3++SO2+2H2O = 2Fe2++SO42-+4H+
(4)不正确,因为分解有O2和SO2生成,在水溶液中发生反应:2SO2+O2+2H2O = 2H2SO4,故无论分解反应是否有SO3生成,都会有此现象
题目分析:同样的根据试验的现象分析综合,可以得到以下信息:①中现象D试管中有无色液体,已知:SO2熔点–72℃,沸点–10℃;SO3熔点16.8℃,沸点44.8℃。所以生成物肯定有SO2。①中现象A中固体变为红棕色,生成了Fe2O3③充分反应,停止加热,冷却后,取A中固体,加盐酸,固体溶解,溶液呈黄色是FeCl3。
②中用带有火星的木条靠近装置D的导管口,木条复燃,肯定有O2。所以基本点信息就可以确定。
(1)实验③反应的离子方程式是Fe2O3+6H+=2Fe3++3H2O(2)分解过程除产生使木条复燃的气体外,仅由A中固体颜色变化推测,还一定有SO2气体,依据是因为有Fe2O3生成,在FeSO4中只有+6价S元素有氧化性,能被还原。因此一定有SO2生成(3)实验④反应的离子方程式是2Fe3++SO2+2H2O = 2Fe2++SO42-+4H+(4)某同学依据B中的现象,认为FeSO4分解一定有SO3生成。不正确,因为分解有O2和SO2生成,在水溶液中发生反应:2SO2+O2+2H2O = 2H2SO4,故无论分解反应是否有SO3生成,都会有此现象。
点评:对实验目的,过程,现象,结论的具体分析找到突破口,联系结点,达到解决的目的。也是高考对学生实验综合素质、化学实验的分析理解能力的考查。
