已知X为FeO和CuO的混合物,取两份等质量的X样品如右图所示的实验:设③中所得固体D的质量为32克,溶液E中只含有一种金属离子,且有酸剩余,气体F的质量为0.5克,试计算取用的每份X的质量,及X中FeO和CuO的质量比.
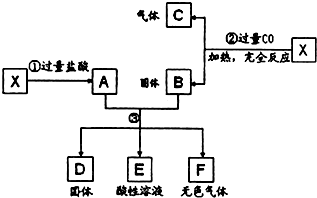
两份X样品的质量相等,则固体D铜的一半16g为CuO与CO反应生成的铜,另一半则为铁与氯化铜反应生成的铜,则混合物X中氧化铜的质量=
÷32g 2
×100%=20g;64 80
设与氯化铜反应的铁的质量为x,与盐酸反应的铁的质量为y
Fe+CuCl2═Cu+FeCl2
56 64
x 16g
=56 64
x=14gx 16g
Fe+2HCl═FeCl2+H2↑
56 2
y 0.5g
=56 2
y=14gy 0.5g
则固体B中铁的质量为14g+14g=28g,混合物X中FeO的质量=28g÷
×100%=36g56 72
每份X的质量=36g+20g=56g,X中FeO和CuO的质量比=36g:20g=9:5
答:每份X的质量为56g,及X中FeO和CuO的质量比为9:5.
