(12分)铁是人类使用最广泛的金属。
(1)一氧化碳在高温下可与氧化铁发生反应;

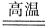 2Fe+3CO
2Fe+3CO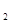 ,此反应可用于工业上冶炼金属铁。反应中,作为氧化剂的物质是________(填化学式)。在该反应中,若消耗了1 mol
,此反应可用于工业上冶炼金属铁。反应中,作为氧化剂的物质是________(填化学式)。在该反应中,若消耗了1 mol 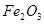 ,则转移了_____mol电子,生成的CO
,则转移了_____mol电子,生成的CO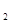 在标准状况下的体积是_________L。
在标准状况下的体积是_________L。
(2)下图是铁粉和水蒸气反应的实验装置示意图,写出该反应的化学方程式_______;实验中,D处排出的气体几乎点不着,已知该装置不漏气,使用的各种药品没有质量问题,你认为气体点不着的可能原因是(说出一点即可):_______________;改正的措施是:_________________。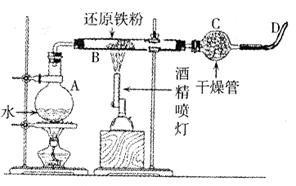
(12分)(每空2分)(1)Fe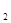 O
O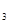 6 67.2
6 67.2
(2)3Fe+4H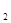 O(g)
O(g)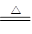 Fe
Fe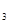 O
O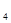 +4H
+4H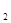
①产生的H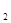 太少 ②水蒸气过多(说出一点即可)
太少 ②水蒸气过多(说出一点即可)
①增加还原铁粉的用量 ②控制烧瓶加热温度,避免产生大量的水蒸气(或增加干燥剂用量)
题目分析:(1)根据方程式可知,铁元素的化合价从+3价降低到0价,得到3个电子,所以氧化铁是氧化剂。1mol氧化铁得到3mol×2=6mol电子。生成3molCO2,所以CO2的体积是67.2L。
(2)高温下,铁和水蒸气反应生成四氧化三铁和氢气,反应的化学方程式是3Fe+4H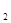 O(g)
O(g)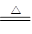 Fe
Fe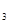 O
O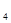 +4H
+4H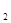 。装置不漏气,使用的各种药品没有质量问题,因此不能点着的原因可能是产生的氢气太少或水蒸气过多引起的。所以改进的措施是增加还原铁粉的用量或控制烧瓶加热温度,避免产生大量的水蒸气(或增加干燥剂用量)。
。装置不漏气,使用的各种药品没有质量问题,因此不能点着的原因可能是产生的氢气太少或水蒸气过多引起的。所以改进的措施是增加还原铁粉的用量或控制烧瓶加热温度,避免产生大量的水蒸气(或增加干燥剂用量)。
点评:该题是基础性试题的考查,试题基础性强,难易适中。该题中实验的考查主要是以实验基本操作为中心,通过是什么、为什么和怎样做重点考查实验基本操作的规范性和准确及灵活运用知识解决实际问题的能力。
