实验室中现有一种固体混合物,其中可能含有Mg、Na2SO4、Na2CO3、BaCl2、BaSO4五种物质中的两种或多种.按下图所示进行实验,出现的现象如图中所述.(设过程中所有发生的反应都恰好完全反应)
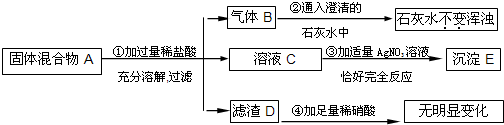
试根据实验过程和发生的现象判断:
(1)产生的气体B是(写化学式)______.
(2)混合物A中,一定存在的物质是(写化学式)______.
(3)在溶液C中,肯定存在的阳离子是(写离子符号)______.
(4)固体混合物里,上述五种物质中,一定不存在的物质是(写化学式)______,得此结论的理由是______.
(5)写出步骤③中一定发生的一个化学反应的方程式:______.
(1)所给的物质中加入盐酸后能产生气体的有:镁和碳酸钠,镁与盐酸反应生成氯化镁和氢气,碳酸钠与盐酸反应生成氯化钠、水、二氧化碳;产生的气体不能使澄清石灰水变浑浊,所以不能是二氧化碳,气体B只能是氢气;
(2)由上题的分析可知生成的气体是氢气,即混合物中含有镁,加入过量盐酸后有滤渣,说明该物质与盐酸不反应,且不溶于水,也不与硝酸反应,硫酸钡符合这一条件,但是如果混合物中含有硫酸钠和氯化钡时,也能生成硫酸钡,所以是否含有硫酸钡,不能确定,所以一定含有镁;
(3)镁与盐酸反应生成氯化镁和氢气,氯化镁中阳离子是镁离子,由于加入的盐酸过量,所以其中含有氢离子;
(4)产生的气体不能使澄清石灰水变浑浊,说明气体不能是二氧化碳,即不能存在碳酸钠,因为碳酸钠与盐酸反应生成氯化钠、水、二氧化碳;
(5)由于镁与盐酸反应生成氯化镁和氢气,所以加入硝酸银后,氯化镁与硝酸银反应,生成氯化银沉淀和硝酸镁,用观察法配平,氯化银后面标上沉淀符号;由于加入盐酸过量,所以还发生了盐酸和硝酸银反应,生成氯化银和硝酸,氯化银后面标上沉淀符号.
故答案为:(1)H2;(2)Mg;(3)Mg2+、H+;(4)Na2CO3;气体B通入澄清石灰水中,没变浑浊;
(5)MgCl2+2AgNO3═2AgCl↓+Mg(NO3)2(或HCl+AgNO3═AgCl↓+HNO3).

 分别表示不同元素的原子),下列对图示反应的理解中,正确的是
分别表示不同元素的原子),下列对图示反应的理解中,正确的是